YBB 0013-2002
基本信息
标准号: YBB 0013-2002
中文名称:药品包装用复合膜、袋通则
标准类别:冶金行业标准(YB)
英文名称:Yaopinbaozhuangyong Fuhemo、Dai Tongze General Rule for Laminated Films and Pouches for Pharmaceutical Packaging
标准状态:已作废
发布日期:2002-07-11
实施日期:2002-12-01
作废日期:2015-12-01
下载格式:pdf zip

标准分类号
标准ICS号: 医药卫生技术>>11.020医学科学和保健装置综合
中标分类号:医药、卫生、劳动保护>>医药、卫生、劳动保护综合>>C08标志、包装、运输、贮存
关联标准
替代情况:被YBB00132002-2015代替
出版信息
页数:9页
标准价格:14.0
出版日期:2002-12-01
相关单位信息
标准简介
本标准适用于非注射剂用的药品包装用复合膜、袋。
标准图片预览

标准内容
国家药品监督管理局
国家药品包装容器(材料)标准
(试行)
药品包装用复合膜、袋通则
YaopinbaozhuangyongFuhemo、DaiTongzeYBB00132002
General Rulefor LaminatedFilms and Pouches forPharmaceutical Packaging复合膜系指各种塑料与纸、金属或其它塑料通过黏合剂组合而形成的膜,其厚度一般不大于0.25mm。
复合袋系将复合膜通过热合的方法而制成的袋,按制袋形式可分为三边封袋、中封袋、风琴袋、自立袋、拉链袋等。本标准适用于非注射剂用的药品包装用复合膜、袋。药品包装用复合膜按材料组合分类,如表1所示:66
纸、塑料
塑料、镀铝膜
纸、铝箔、塑料
塑料(非单层)、
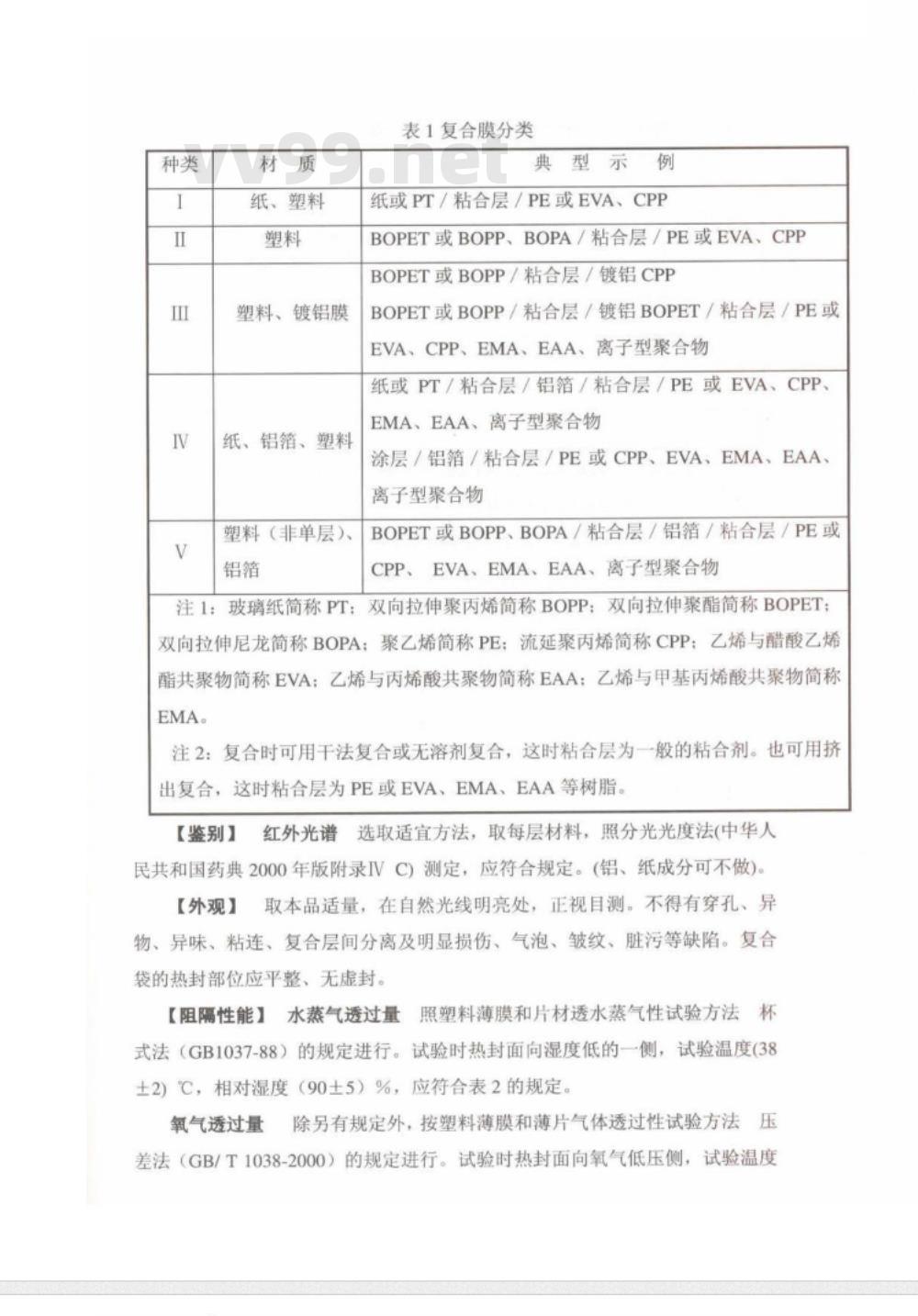
表1复合膜分类
典型示例
纸或PT/粘合层/PE或EVA、CPP
BOPET或BOPP、BOPA/粘合层/PE或EVA、CPPBOPET或BOPP/粘合层/镀铝CPP
BOPET或BOPP/粘合层/镀铝BOPET/粘合层/PE或EVA、CPP、EMA、EAA、离子型聚合物纸或PT/粘合层/铝箔/粘合层/PE或EVA、CPP、EMA、EAA、离子型聚合物
涂层/铝箔/粘合层/PE或CPP、EVA、EMA、EAA、离子型聚合物
BOPET或BOPP、BOPA/粘合层/铝箔/粘合层/PE或CPP、EVA、EMA、EAA、离子型聚合物双向拉伸聚丙烯简称BOPP:双向拉伸聚酯简称BOPET:注1:玻璃纸简称PT:
双向拉伸尼龙简称BOPA:聚乙烯简称PE:流延聚丙烯简称CPP:乙烯与醋酸乙烯酯共聚物简称EVA:乙烯与丙烯酸共聚物简称EAA:乙烯与甲基丙烯酸共聚物简称EMA。
注2:复合时可用干法复合或无溶剂复合,这时粘合层为一般的粘合剂。也可用挤出复合,这时粘合层为PE或EVA、EMA、EAA等树脂。【鉴别】
红外光谱选取适宜方法,取每层材料,照分光光度法(中华人民共和国药典2000年版附录IVC)测定,应符合规定。(铝、纸成分可不做)。【外观】
取本品适量,在自然光线明亮处,正视目测。不得有穿孔、异物、异味、粘连、复合层间分离及明显损伤、气泡、皱纹、脏污等缺陷。复合袋的热封部位应平整、无虚封。【阻隔性能】水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88)的规定进行。试验时热封面向湿度低的一侧,试验温度(38土2)℃,相对湿度(90土5)%,应符合表2的规定。氧气透过量
除另有规定外,按塑料薄膜和薄片气体透过性试验方法压
差法(GB/T1038-2000)的规定进行。试验时热封面向氧气低压侧,试验温度(23土2)℃,应符合表2的规定。种类
【机械性能】
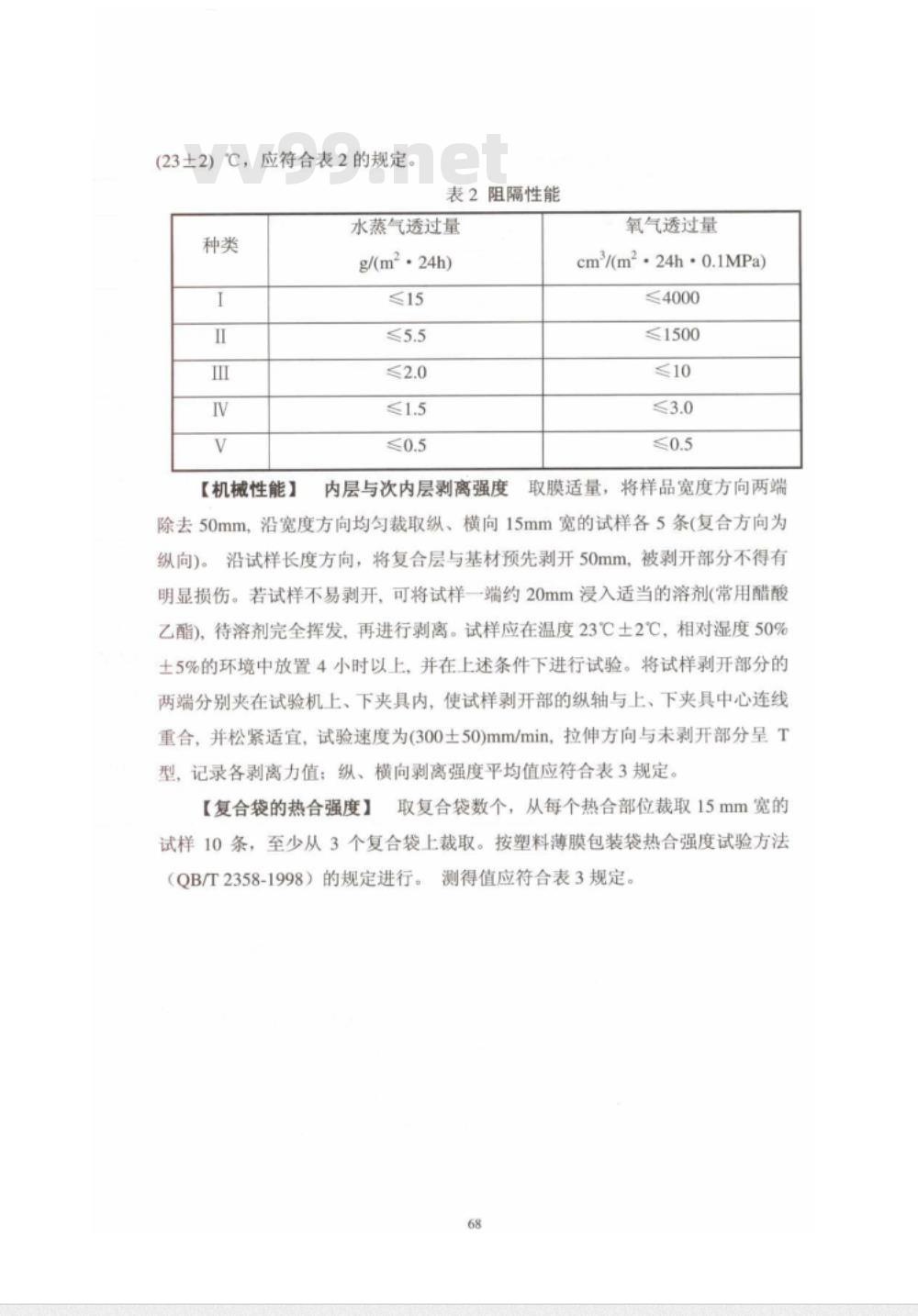
表2阻隔性能
水蒸气透过量
g/(m2·24h)
氧气透过量
cm2/(m2·24h·0.1MPa)
≤4000
≤1500
内层与次内层剥离强度取膜适量,将样品宽度方向两端除去50mm,沿宽度方向均匀裁取纵、横向15mm宽的试样各5条(复合方向为纵向)。沿试样长度方向,将复合层与基材预先剥开50mm,被剥开部分不得有明显损伤。若试样不易剥开,可将试样一端约20mm浸入适当的溶剂(常用醋酸乙酯),待溶剂完全挥发,再进行剥离。试样应在温度23℃土2℃,相对湿度50%土5%的环境中放置4小时以上,并在上述条件下进行试验。将试样剥开部分的两端分别夹在试验机上、下夹具内,使试样剥开部的纵轴与上、下夹具中心连线重合,并松紧适宜,试验速度为(300土50)mm/min,拉伸方向与未剥开部分呈T型,记录各剥离力值:纵、横向剥离强度平均值应符合表3规定。取复合袋数个,从每个热合部位裁取15mm宽的【复合袋的热合强度】
试样10条,至少从3个复合袋上裁取。按塑料薄膜包装袋热合强度试验方法(QB/T2358-1998)的规定进行。测得值应符合表3规定。68
内层与次内层剥离
热合强度
【溶剂残留量】
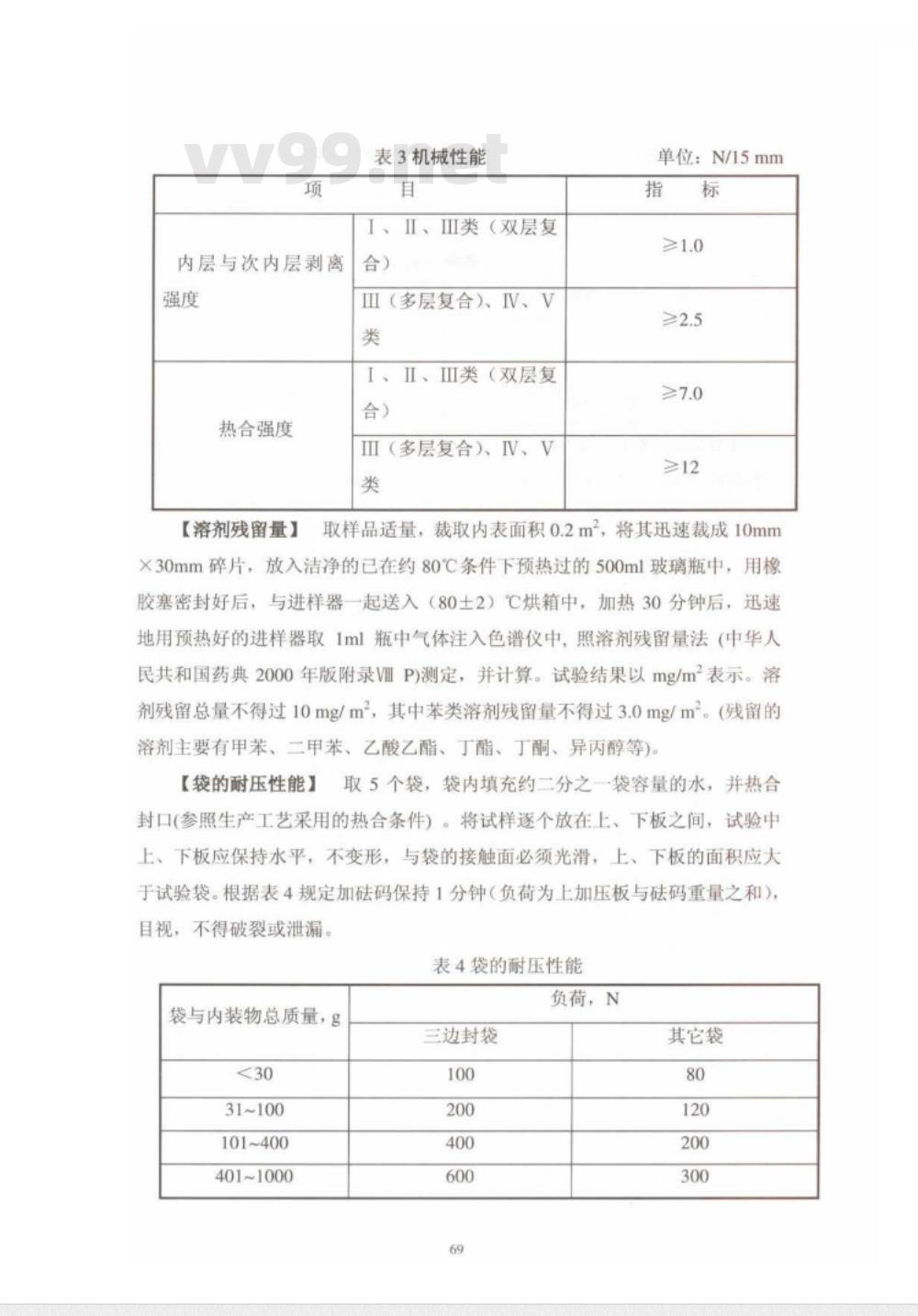
表3机械性能
I、II、Ⅲ类(双层复
ⅢI(多层复合)、IN、V
I、Ⅱ、Ⅱ类(双层复
Ⅲ(多层复合))、IV、V
单位:N/15mm
≥>12
取样品适量,裁取内表面积0.2m2,将其迅速裁成10mm×30mm碎片,放入洁净的已在约80℃条件下预热过的500ml玻璃瓶中,用橡胶塞密封好后,与进样器一起送入(80土2)℃烘箱中,加热30分钟后,迅速地用预热好的进样器取1ml瓶中气体注入色谱仪中,照溶剂残留量法(中华人民共和国药典2000年版附录VIlP)测定,并计算。试验结果以mg/m2表示。溶剂残留总量不得过10mg/m2,其中苯类溶剂残留量不得过3.0mg/m。(残留的溶剂主要有甲苯、二甲苯、乙酸乙酯、丁酯、丁酮、异丙醇等)。【袋的耐压性能】取5个袋,袋内填充约二分之一袋容量的水,并热合封口(参照生产工艺采用的热合条件)。将试样逐个放在上、下板之间,试验中上、下板应保持水平,不变形,与袋的接触面必须光滑,上、下板的面积应大于试验袋。根据表4规定加码保持1分钟(负荷为上加压板与码重量之和)目视,不得破裂或泄漏。
表4袋的耐压性能
袋与内装物总质量,g
31~100
101~400
401~1000
三边封袋
负荷,N
其它袋
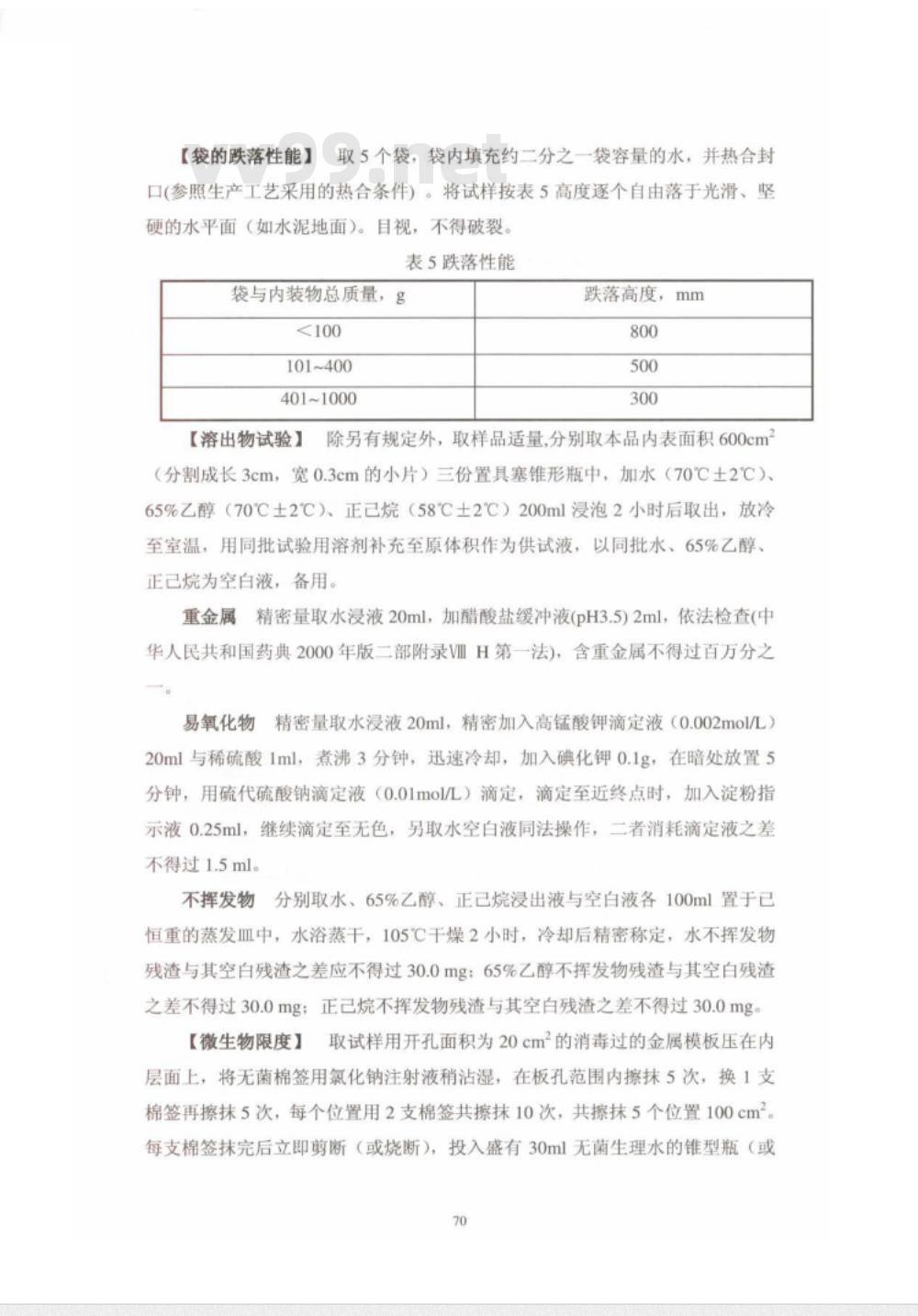
【袋的跌落性能】取5个袋,袋内填充约二分之一袋容量的水,并热合封口(参照生产工艺采用的热合条件)。将试样按表5高度逐个自由落于光滑、坚硬的水平面(如水泥地面)。目视,不得破裂。表5跌落性能
袋与内装物总质量,g
101~400
401~1000
跌落高度,mm
1除另有规定外,取样品适量,分别取本品内表面积600cm【溶出物试验】
(分割成长3cm,宽0.3cm的小片)三份置具塞锥形瓶中,加水(70℃土2℃)、65%乙醇(70℃土2℃)、正已烷(58℃土2℃)200ml浸泡2小时后取出,放冷至室温,用同批试验用溶剂补充至原体积作为供试液,以同批水、65%乙醇、正已烷为空白液,备用。
重金属精密量取水浸液20ml,加醋酸盐缓冲液(pH3.5)2ml,依法检查(中华人民共和国药典2000年版二部附录VIH第一法),含重金属不得过百万分之。
易氧化物
精密量取水浸液20ml,精密加入高锰酸钾滴定液(0.002mol/L)20ml与稀硫酸1ml,煮沸3分钟,迅速冷却,加入碘化钾0.1g,在暗处放置5分钟,用硫代硫酸钠滴定液(0.01mol/L)滴定,滴定至近终点时,加入淀粉指示液0.25ml,继续滴定至无色,另取水空白液同法操作,二者消耗滴定液之差不得过1.5ml。
不挥发物
分别取水、65%乙醇、正已烷浸出液与空白液各100ml置于已恒重的蒸发皿中,水浴蒸干,105℃干燥2小时,冷却后精密称定,水不挥发物残渣与其空白残渣之差应不得过30.0mg65%乙醇不挥发物残渣与其空白残渣之差不得过30.0mg;正已烷不挥发物残渣与其空白残渣之差不得过30.0mg1取试样用开孔面积为20cm2的消毒过的金属模板压在内【微生物限度】vv99.net
层面上,将无菌棉签用氯化钠注射液稍沾湿,在板孔范围内擦抹5次,换1支棉签再擦抹5次,每个位置用2支棉签共擦抹10次,共擦抹5个位置100cm2。每支棉签抹完后立即剪断(或烧断),投入盛有30ml无菌生理水的锥型瓶(或70
大试管)中。全部擦抹棉签投入瓶中后,将瓶迅速摇晃1分钟,即得供试液。取提取液照微生物限度法(中华人民共和国药典2000年版二部附录XIJ)测定。应符合表6的规定。
表6微生物限度指标
细菌数
个/100cm2
霉菌、酵母菌数
个/100cm2
大肠杆菌
金黄色葡萄球菌
铜绿假单胞菌
一般复合膜、袋
外用药复合膜、袋
注:“一”为每100cm2中不得检出。100
栓剂用复合膜、袋
【异常毒性】
取试样500cm2,剪碎,加入氯化钠注射液50ml,110℃湿
热灭菌30分钟后取出,冷却备用,静脉注射,依法测定(中华人民共和国药典2000年版二部附录XIC),应符合规定附件:
检验规则
」外观检验:复合膜按每卷膜取2米进行检验:复合袋按逐批检查计数抽样程序及抽样表(GB/T2828一87)规定进行,检查水平为一般检查水平II,合格质量水平(AOL)为6.5。表7尺寸偏差
厚度偏差,%
平均厚度偏差,%
热封宽度偏差,%
热合边与袋边的距离,
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
国家药品包装容器(材料)标准
(试行)
药品包装用复合膜、袋通则
YaopinbaozhuangyongFuhemo、DaiTongzeYBB00132002
General Rulefor LaminatedFilms and Pouches forPharmaceutical Packaging复合膜系指各种塑料与纸、金属或其它塑料通过黏合剂组合而形成的膜,其厚度一般不大于0.25mm。
复合袋系将复合膜通过热合的方法而制成的袋,按制袋形式可分为三边封袋、中封袋、风琴袋、自立袋、拉链袋等。本标准适用于非注射剂用的药品包装用复合膜、袋。药品包装用复合膜按材料组合分类,如表1所示:66
纸、塑料
塑料、镀铝膜
纸、铝箔、塑料
塑料(非单层)、
表1复合膜分类
典型示例
纸或PT/粘合层/PE或EVA、CPP
BOPET或BOPP、BOPA/粘合层/PE或EVA、CPPBOPET或BOPP/粘合层/镀铝CPP
BOPET或BOPP/粘合层/镀铝BOPET/粘合层/PE或EVA、CPP、EMA、EAA、离子型聚合物纸或PT/粘合层/铝箔/粘合层/PE或EVA、CPP、EMA、EAA、离子型聚合物
涂层/铝箔/粘合层/PE或CPP、EVA、EMA、EAA、离子型聚合物
BOPET或BOPP、BOPA/粘合层/铝箔/粘合层/PE或CPP、EVA、EMA、EAA、离子型聚合物双向拉伸聚丙烯简称BOPP:双向拉伸聚酯简称BOPET:注1:玻璃纸简称PT:
双向拉伸尼龙简称BOPA:聚乙烯简称PE:流延聚丙烯简称CPP:乙烯与醋酸乙烯酯共聚物简称EVA:乙烯与丙烯酸共聚物简称EAA:乙烯与甲基丙烯酸共聚物简称EMA。
注2:复合时可用干法复合或无溶剂复合,这时粘合层为一般的粘合剂。也可用挤出复合,这时粘合层为PE或EVA、EMA、EAA等树脂。【鉴别】
红外光谱选取适宜方法,取每层材料,照分光光度法(中华人民共和国药典2000年版附录IVC)测定,应符合规定。(铝、纸成分可不做)。【外观】
取本品适量,在自然光线明亮处,正视目测。不得有穿孔、异物、异味、粘连、复合层间分离及明显损伤、气泡、皱纹、脏污等缺陷。复合袋的热封部位应平整、无虚封。【阻隔性能】水蒸气透过量照塑料薄膜和片材透水蒸气性试验方法杯式法(GB1037-88)的规定进行。试验时热封面向湿度低的一侧,试验温度(38土2)℃,相对湿度(90土5)%,应符合表2的规定。氧气透过量
除另有规定外,按塑料薄膜和薄片气体透过性试验方法压
差法(GB/T1038-2000)的规定进行。试验时热封面向氧气低压侧,试验温度(23土2)℃,应符合表2的规定。种类
【机械性能】
表2阻隔性能
水蒸气透过量
g/(m2·24h)
氧气透过量
cm2/(m2·24h·0.1MPa)
≤4000
≤1500
内层与次内层剥离强度取膜适量,将样品宽度方向两端除去50mm,沿宽度方向均匀裁取纵、横向15mm宽的试样各5条(复合方向为纵向)。沿试样长度方向,将复合层与基材预先剥开50mm,被剥开部分不得有明显损伤。若试样不易剥开,可将试样一端约20mm浸入适当的溶剂(常用醋酸乙酯),待溶剂完全挥发,再进行剥离。试样应在温度23℃土2℃,相对湿度50%土5%的环境中放置4小时以上,并在上述条件下进行试验。将试样剥开部分的两端分别夹在试验机上、下夹具内,使试样剥开部的纵轴与上、下夹具中心连线重合,并松紧适宜,试验速度为(300土50)mm/min,拉伸方向与未剥开部分呈T型,记录各剥离力值:纵、横向剥离强度平均值应符合表3规定。取复合袋数个,从每个热合部位裁取15mm宽的【复合袋的热合强度】
试样10条,至少从3个复合袋上裁取。按塑料薄膜包装袋热合强度试验方法(QB/T2358-1998)的规定进行。测得值应符合表3规定。68
内层与次内层剥离
热合强度
【溶剂残留量】
表3机械性能
I、II、Ⅲ类(双层复
ⅢI(多层复合)、IN、V
I、Ⅱ、Ⅱ类(双层复
Ⅲ(多层复合))、IV、V
单位:N/15mm
≥>12
取样品适量,裁取内表面积0.2m2,将其迅速裁成10mm×30mm碎片,放入洁净的已在约80℃条件下预热过的500ml玻璃瓶中,用橡胶塞密封好后,与进样器一起送入(80土2)℃烘箱中,加热30分钟后,迅速地用预热好的进样器取1ml瓶中气体注入色谱仪中,照溶剂残留量法(中华人民共和国药典2000年版附录VIlP)测定,并计算。试验结果以mg/m2表示。溶剂残留总量不得过10mg/m2,其中苯类溶剂残留量不得过3.0mg/m。(残留的溶剂主要有甲苯、二甲苯、乙酸乙酯、丁酯、丁酮、异丙醇等)。【袋的耐压性能】取5个袋,袋内填充约二分之一袋容量的水,并热合封口(参照生产工艺采用的热合条件)。将试样逐个放在上、下板之间,试验中上、下板应保持水平,不变形,与袋的接触面必须光滑,上、下板的面积应大于试验袋。根据表4规定加码保持1分钟(负荷为上加压板与码重量之和)目视,不得破裂或泄漏。
表4袋的耐压性能
袋与内装物总质量,g
31~100
101~400
401~1000
三边封袋
负荷,N
其它袋
【袋的跌落性能】取5个袋,袋内填充约二分之一袋容量的水,并热合封口(参照生产工艺采用的热合条件)。将试样按表5高度逐个自由落于光滑、坚硬的水平面(如水泥地面)。目视,不得破裂。表5跌落性能
袋与内装物总质量,g
101~400
401~1000
跌落高度,mm
1除另有规定外,取样品适量,分别取本品内表面积600cm【溶出物试验】
(分割成长3cm,宽0.3cm的小片)三份置具塞锥形瓶中,加水(70℃土2℃)、65%乙醇(70℃土2℃)、正已烷(58℃土2℃)200ml浸泡2小时后取出,放冷至室温,用同批试验用溶剂补充至原体积作为供试液,以同批水、65%乙醇、正已烷为空白液,备用。
重金属精密量取水浸液20ml,加醋酸盐缓冲液(pH3.5)2ml,依法检查(中华人民共和国药典2000年版二部附录VIH第一法),含重金属不得过百万分之。
易氧化物
精密量取水浸液20ml,精密加入高锰酸钾滴定液(0.002mol/L)20ml与稀硫酸1ml,煮沸3分钟,迅速冷却,加入碘化钾0.1g,在暗处放置5分钟,用硫代硫酸钠滴定液(0.01mol/L)滴定,滴定至近终点时,加入淀粉指示液0.25ml,继续滴定至无色,另取水空白液同法操作,二者消耗滴定液之差不得过1.5ml。
不挥发物
分别取水、65%乙醇、正已烷浸出液与空白液各100ml置于已恒重的蒸发皿中,水浴蒸干,105℃干燥2小时,冷却后精密称定,水不挥发物残渣与其空白残渣之差应不得过30.0mg65%乙醇不挥发物残渣与其空白残渣之差不得过30.0mg;正已烷不挥发物残渣与其空白残渣之差不得过30.0mg1取试样用开孔面积为20cm2的消毒过的金属模板压在内【微生物限度】vv99.net
层面上,将无菌棉签用氯化钠注射液稍沾湿,在板孔范围内擦抹5次,换1支棉签再擦抹5次,每个位置用2支棉签共擦抹10次,共擦抹5个位置100cm2。每支棉签抹完后立即剪断(或烧断),投入盛有30ml无菌生理水的锥型瓶(或70
大试管)中。全部擦抹棉签投入瓶中后,将瓶迅速摇晃1分钟,即得供试液。取提取液照微生物限度法(中华人民共和国药典2000年版二部附录XIJ)测定。应符合表6的规定。
表6微生物限度指标
细菌数
个/100cm2
霉菌、酵母菌数
个/100cm2
大肠杆菌
金黄色葡萄球菌
铜绿假单胞菌
一般复合膜、袋
外用药复合膜、袋
注:“一”为每100cm2中不得检出。100
栓剂用复合膜、袋
【异常毒性】
取试样500cm2,剪碎,加入氯化钠注射液50ml,110℃湿
热灭菌30分钟后取出,冷却备用,静脉注射,依法测定(中华人民共和国药典2000年版二部附录XIC),应符合规定附件:
检验规则
」外观检验:复合膜按每卷膜取2米进行检验:复合袋按逐批检查计数抽样程序及抽样表(GB/T2828一87)规定进行,检查水平为一般检查水平II,合格质量水平(AOL)为6.5。表7尺寸偏差
厚度偏差,%
平均厚度偏差,%
热封宽度偏差,%
热合边与袋边的距离,
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。