YY 0304-1998
基本信息
标准号: YY 0304-1998
中文名称:等离子喷涂羟基磷灰石涂层-钛基牙种植体
标准类别:医药行业标准(YY)
英文名称:Plasma sprayed hydroxyapatite coated titanium dental implant
标准状态:已作废
发布日期:1998-04-08
实施日期:1998-10-01
作废日期:2011-06-01
下载格式:pdf zip

标准分类号
中标分类号:医药、卫生、劳动保护>>医疗器械>>C33口腔科器械、设备与材料
出版信息
出版社:中国标准出版社
书号:155066.2-12368
页数:13页
标准价格:21.0
出版日期:2004-04-23
相关单位信息
起草人:陈继镛、张兴栋、刘晓光、朱蔚精
起草单位:四川大学生物材料工程研究中心
归口单位:全国口腔材料和器械设备标准化技术委员会
提出单位:国家医药管理局
发布部门:国家医药管理局
标准简介
本标准规定了等离子喷涂羟基磷灰石涂层一钛基牙种植体的技术要求、试验方法、产品分类、抽样、标志、标签、包装、运输及贮存等要求。
本标准适用于牙缺失后颌骨内植入的等离子喷涂的羟基磷灰石涂层一钛基牙种植体。
标准图片预览




标准内容
YY0304--1998
等离子喷涂羟基磷灰石涂层-钛基牙种植体是由纯钛基体和其表面的羟基磷灰石涂层构成。本标准对于羟基磷灰石涂层性能指标和检测方法,主要参照美国食品和药品管理局(FDA)1992年11月11日发布的《FDA磷酸钙(Ca-P)涂层矫形种植体和骨内种植体申请认可指南》制定;对于制作基体的钛和钛合金性能指标和检测方法,则采用GB3620.2-94《钛和钛合金加工产品化学成分及成分允许偏差》中关于TA2、TA3和TC4的规定,此规定基本符合美国试验和材料学会ASTMF67:1989(1994年重新认可版本)《外科植人用钛的技术规范标准》,ASTM1341:1992《外科植人用钛丝的技术规范标准》和F136《外科植人用缎造6A1-4VELI钛合金技术规范》;对于材料的生物学评价项目选取,按YY0268一1995《口腔材料生物学评价第1单元:口腔材料生物性能评价导则》规定,生物学试验方法尽可能采用国家标准和行业标准,见附录A。A7骨植人试验参照ASTMF981:1986,《用于外科植人的无孔生物材料相容性评价(有关材料对肌肉和骨骼的作用)的实施标准》进行。HA涂层-钛基抗拉强度试验方法采用ASTMF1501:1994《磷酸钙涂层抗拉强度测试方法》,见附录C。临床应用的牙种植体具有多种形态和结构,本标准不可能对其分别作出具体规定,仅列出几种主要形态牙种植体的几何尺寸精度要求。等离子喷涂羟基磷灰石涂层-钛基牙种植体的生物学性能,不仅与材料系统有关,而且与其形态和结构设计密切相关。任何形态和结构未获市场准人的牙种植体,都应进行动物和临床试验,临床跟踪考察不得少于三年。不论牙种植体采用何种形态和结构,所有等离子喷涂羟基磷灰石涂层-钛基牙种植体都必须满足本标准规定的技术要求本标准的附录A、附录B、附录C和附录D均是标准的附录。本标准由国家医药管理局提出。本标准由全国口腔材料和器械设备标准化技术委员会归口。本标准起草单位:四川大学生物材料工程研究中心。本标准主要起草人:陈继镛、张兴栋、刘晓光、朱蔚精。151
1范围
中华人民共和国医药行业标准
等离子喷涂
羟基磷灰石涂层-钛基牙种植体
Plasma sprayed
hydroxyapatite coated titanium dental implantYY 0304-1998
本标准规定了等离子喷涂羟基磷灰石涂层-钛基牙种植体的技术要求、试验方法、产品分类、抽样、标志、标签、包装、运输及贮存等要求。本标准适用于牙缺失后颌骨内植入的等离子喷涂的羟基磷灰石涂层-钛基牙种植体。2引用标准
下列标准所包含的条文,通过在本标准中引用而构成本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。包装储运图示标志
GB 191—901
逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB 2828--87
GB 2829-87
周期检查计数抽样程序及抽样表(适用于生产过程稳定性的检查)GB3620.1-—94钛及钛合金牌号和化学成分钛及钛合金加工产品化学成分及成分允许偏差GB 3620. 2--94
GB 4698—1996
钛和钛合金化学分析方法
3化学试剂火焰原子吸收光谱法通则GB 9723—88
GB 10724—89
GB 11749--89
无火焰(石墨炉)原子吸收光谱法通则化学试剂
牙科复合树脂充填材料
YY/T0127.1-—93口腔材料生物试验方法溶血试验
YY/T 0127.2—93
YY/T 0244--1996
YY/T 0279--1995
静脉注射急性全身毒性试验
口腔材料生物试验方法
口腔材料生物试验方法
经口途径
短期全身毒性试验
口腔粘膜刺激试验
口腔材料生物试验方法
YY0268—1995口腔材料生物学评价第1单元:口腔材料生物性能评价导则中华人民共和国药典(1995年版)3定义
本标准采用下列定义。
3.1牙种植体dental implants
一类植入牙床组织内,用以支持义齿或固定松动牙的中间修复体。它可以根据需要做成圆柱状、叶片状和螺旋状等多种形态,植人粘膜内、骨内、骨膜下、根管内等牙床中不的部位。牙种植体可以由金属、陶瓷、聚合物或天然物质等不同材料所构成或由前述材料复合而成。国家医药管理局1998-04-08批准152
1998-10-01实施
YY0304—1998
3.2羟基磷灰石涂层hydroxyapatite coating利用热喷涂、沉积或烧结等不同方法,在金属、陶瓷或其他材料基体表面上形成的羟基磷灰石(HA)薄层。
3.3等离子喷涂plasma spraying热喷涂工艺的一种,是使用非转移型电弧作为热源使气体离子化,从而产生高达10000℃以上的高温,使通过喷枪送人等离子焰的喷涂材料粉料熔融或表面熔融并高速喷射到基体表面上形成涂层的方法。
3.4粘结强度adhesive strength涂层和基体间单位面积粘着力的大小。根据测试时外加载荷方向是垂直或平行于涂层-基体界面,粘结强度又可分为抗拉强度(tensile strength)和剪切强度(shear strength)。3.5HA涂层结晶度crystallinityHA涂层通常都同时包含结晶相和非晶相,HA涂层中结晶相所占百分比称为结晶度。4要求
4.1几何尺寸精度
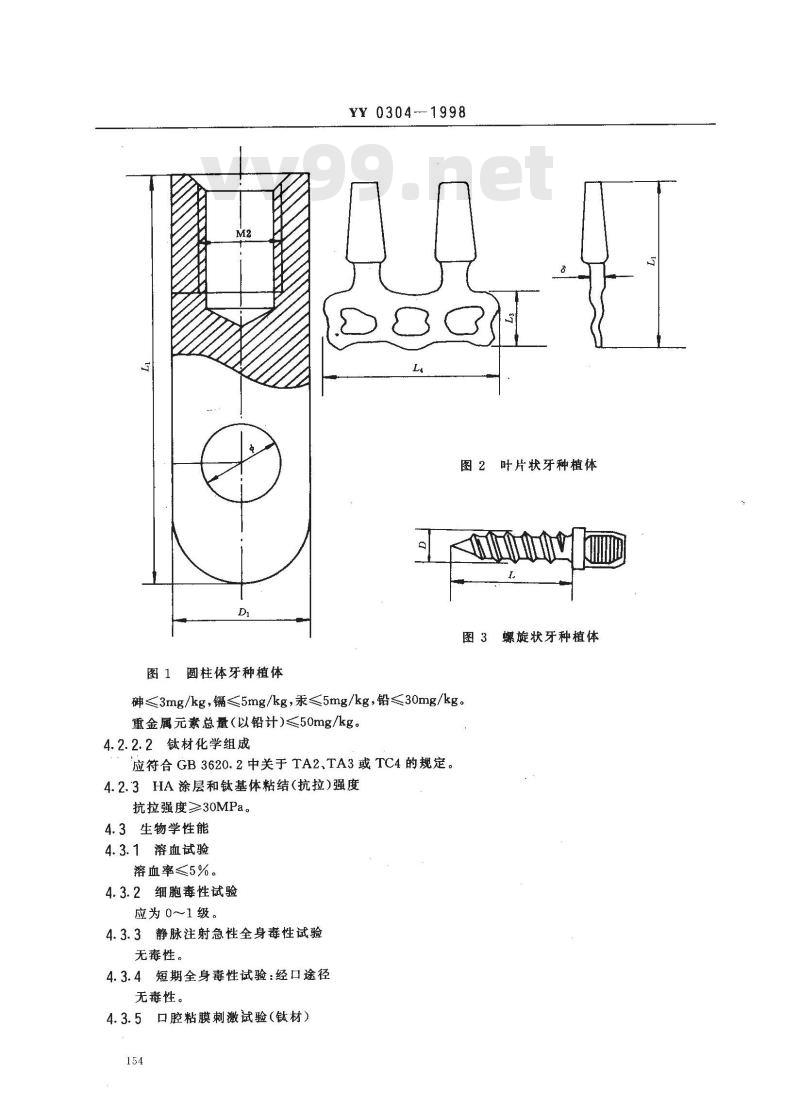
等离子喷涂羟基磷灰石涂层-钛基牙种植体,是由植入牙槽骨内的根部及用以装设义齿的冠桩所构成。按其形态可分为圆柱状、叶片状和螺旋状等多种类型,每一类型又可按结构分为冠桩不可拆卸和冠桩可拆卸两种类型。临床使用的种植体形态和结构种类很多,其典型形态和结构如图1、图2和图3所示。通常是植入牙槽骨内的根部表面为羟基磷灰石涂层覆盖,以促进种植体和周围骨组织间的结合。对各种类型的种植体几何尺寸精度要求如下。4.1. 1圆柱状牙种植体(图1)
根部长度L,和直径D均可根据需要设计成不同尺寸,根部长度L,的极限偏差为土0.2mm,根部直径D,的极限偏差为土0.1mm。
4.1.2叶片状牙种植体(图2)
叶片状牙种植体形态和尺寸种类很多,图2所示为二个冠桩的一段式叶片状牙种植体,植入骨内的根部长度L:和宽度L的极限偏差为士0.4mm,肩部厚度3的极限偏差为士0.2mm。4.1.3螺旋状牙种植体(图3)
图3所示为一段式螺旋状牙种植体,其螺纹顶径D的极限偏差为士0.2mm,根部长度L的极限偏差为士0.4mm。
4.1.4螺纹应给出螺纹代号和螺纹公差带代号,其加工精度和公差带规定应保证冠桩可拆卸式种植体的根部和冠桩连结螺纹相互配合良好4.2物理化学性能
4.2.1外观
牙种植体未涂层的钛表面应无裂纹、无毛刺和划痕等机械加工所致的宏观缺陷,两段式种植体的根部和冠桩对中和配合应良好,配合面间无明显可见的间隙和偏移。羟基磷灰石涂层为灰白色多孔薄层,涂层表面色泽均勾并严密复盖钛基体,不得有斑点或裂纹。4.2.2化学组成
4.2.2.1HA涂层的化学组成
4.2.2.1.1涂层中HA含量和结晶度HA含量≥90%,HA结晶度≥62%。4.2.2.1.2杂质元素含量极限
图1圆柱体牙种植体
YY 0304--1998
图2叶片状牙种植体
图3螺旋状牙种植体
砷≤3mg/kg,镉≤5mg/kg,汞≤5mg/kg,铅≤30mg/kg重金属元素总量(以铅计)≤50mg/kg。4.2.2.2钛材化学组成
应符合GB3620.2中关于TA2、TA3或TC4的规定。4.2.3HA涂层和钛基体粘结(抗拉)强度抗拉强度≥30MPa。
4.3生物学性能
4.3.1溶血试验
溶血率≤5%。
4.3.2细胞毒性试验
应为0~1级。
4.3.3静脉注射急性全身毒性试验无毒性。
4.3.4短期全身毒性试验:经口途径无毒性。
4.3.5口腔粘膜刺激试验(钛材)154
无刺激。
4.3.6Ames试验
诱变试验阴性。
4.3.7骨植入应用试验
总毒性比率为1~0级(≤1级)。4.3.8皮下植入试验
埋植12周,无反应或轻度反应。4.3.9致敏试验
无过敏反应。
5试验方法
5.1牙种植体几何尺寸
YY 0304—1998
几何尺寸精度用千分尺或千分表测量,精度:二级,0.01mm士0.001mm。连接螺纹加工精度用螺纹塞规或螺纹环规检验。使用的塞规和环规公差带应与螺纹公差带一致。5.2物理化学性能Www.vV99.net
5.2.1外观
目测法。
5.2.2化学组成
5.2.2.1羟基磷灰石涂层的化学成分5.2.2.1.1涂层HA含量和结晶度
用陪片进行测试,陪片的基底为12mm×12mm×1.5mm的钛片,共三片,按与同批号产品相同的工艺条件在钛片上制作HA涂层,然后记录陪片的X射线衍射谱(XRD谱),HA含量计算按附录D进行。结晶度计算方法见附录B。
5.2.2.1.2HA涂层微量杂质含量和重金属元素总量用与同批号产品相同的喷涂工艺,在清洁钛片上多次重复喷涂HA厚涂层。将厚涂层从钛片上剥离下来进行测试。砷含量测试按《中华人民共和国药典》(1995年版)碑盐检查法;和铅含量测试按GB10724进行;汞含量测试按GB9723进行:重金属元素总量测试按《中华人民共和国药典》(1995年版)附录中重金属检验法进行。
5.2.2.2钛材化学组成
按GB4698规定进行。
5.2.3涂层和钛基体界面抗拉强度抗拉强度检测按附录C进行。
5.3生物学试验
见附录A《等离子喷涂HA-Ti牙种植体生物学试验方法》。6检验规则
6.1每一批产品均应经生产厂技术检验部门进行检查,合格后方可提交验收。6.2产品必须按批号成批提交检查。检查分为逐批检查和周期检查。6.3逐批检查
6.3.1逐批检查按GB2828的规定进行。6.3.2抽样方案类型
采用一次抽样。抽样方案严格性按正常检查抽样方案进行,检查水平为I,缺陷分类、检查项目和AQL(合格质量水平)按表1的规定。采取随机抽样方式抽取被检查的样本。155
缺陷分类
检查项目
6.4周期检查
6.4.1在下列情况下应进行周期检查:a)产品初次投产前;
b)间隔1年以上再投产时;
YY 0304--1998
逐批检查
4.1.1,4.1.4,4.2.1
c)设计、工艺或生产设备有重大改变时。轻
4.1.2,4.1.3
6.4.2对表1所列检查项目,周期检查前应先进行逐批检查,从逐批检查合格的批中抽取样本进行周期检查,周期检查按GB2829进行,采用一次抽样方案,从连续5批产品中,每批随机抽取4个试样,共20个试样组成样本,判定数组和不合格质量水平(RQL)见表2。6.4.3周期检查合格,必须是本周期所有检查项目都合格,否则就认为周期检查不合格。表 2周期检查
检查项目
4.2.2.1.1
4.2.2.1.2
检查周期
6.4.1规定情况
1)6.4.1规定情况;
2)更换喷涂用HA粉批号时
1)6.4.1规定情况;
2)每年一次
1)6.4.1规定情况;
2)每六个月一次
每批钛材购进时
6.4.1规定情况
7标志、标签、包装、运输、贮存判定数组或合格标准
n= 20[A=1,Re= 2]
n- 3A = 0,R --1]
杂质元素含量符合4.2.2.1.2规定算术平均值符合4.2.3规定
符合GB3620.2的有关规定
符合4,3规定
7.1牙种植体必须包装在密封的容器中。容器材料应无毒,不污染和影响牙种植体性能,包装容器还应具有正常搬运或储存期间不损坏、不破裂的性能。7.2内包装上应注明规格、型号、商标和批号。7.3中包装为硬塑料或其他无毒硬质盒。中包装上应注明制造厂名称、商标和地址、产品名称、型号、数量和批号。
7.4每一中包装盒内应附有牙种植体使用说明书,使用说明书应按国家有关规定编写,至少应有下列内容:
a)牙种植体的材质类型;
b)牙种植体消毒方法;
c)临床使用简要说明;
d)牙种植体贮存保管注意事项,YY 0304-1998
e)牙种植体使用过程中可能出现的意外及应采取的措施。5运输包装采用木箱,封装后的成品置于木箱内,内盖用软纸或泡沫塑料填塞。木箱上标明防潮、防7.5
震、远离有害物质等字样或标志。157
A1溶血试验
按 YY/T0127.1。
YY 0304-1998
附录A
(标雅的附录)
等离子喷涂HA-Ti牙种植体生物学试验方法A2细胞毒性试验(分子过滤法)按GB11749--89中 A2。
A3 静脉注射急性全身毒性试验
按 YY/T 0127. 2。
A4短期全身毒性试验:经口途径按 YY/T 0244
A5口腔粘膜刺激试验(钛材)
按 YY/T 0279。
A6 Ames 试验
按GB11749—89中A3,试样为材料浸提液。A7骨植入试验
A7.1范围
本试验适用于外科植入,无吸收的生物材料的组织反应,适用于评价在人体骨骼内停留超过30天,且不被吸收的材料。
A7.2植人试样的制备
A7.2.1将受试材料制备成直径2mm,长6mm圆柱体,表面光洁,同时制备直径2mm,长6mm阴性对照试样。
A7.2.2试样与对照样品经自来水冲洗,超声波清洗两次,0.9%的氧化钠(NaCI)清洗两次,每次约1min,高压蒸汽灭菌。
A7.2.3植入样品的清洁、包装、消毒方式应与产品临床应用一致。A7.3试验动物
选用体重2~2.5kg大白兔。
A7.4植人期间
以相间的外科手术将所有的植人样品,分别植入每只动物,以便使植人期间的组织反应相一致。每时间至少4只大白兔。
A7.5植人步骤
A7.5.1采用灭菌操作技术,暴露动物股骨外侧骨皮质,用符合要求的设备和技术,以2000~3000r/min的速度,在股骨外侧骨皮质上钻三个孔(直径2mm),分别用手指或器械将植人样品压人洞内,每条股骨植人试样2个,对照样1个,然后缝合封闭创口。158
A7.6植入物的取出和动物处死
YY 0304—1998
A7.6、1于植人后1、2、4、8、12、26和52周,动脉放血处死动物,每次4只。A7.6.2观察植人物及其周围组织,记录肉眼所见的改变。A7.6.3将植入物及其周围的骨组织-起取下来,在切取的组织样品中,至少要包含5mm厚的植入物周围组织。
A7.7组织学样品制备
A7.7.1自每一植人部位制备组织块。A7.7.2将组织块置20%甲醛溶液中固定,制备成组织病理切片,切组织片时,应由端到另端同时记录植人样品周围组织的肉眼观察所见。A7.7.3如果需要特殊染色,应另外制备组织块或切片。A7.8组织病理观察
A7.8.1观察试样周围组织的病理反应,并与对照样品周围的组织反应相比较。观察癜痕厚度,炎性细胞或其他种类的细胞以及在试验条件下确实由材料引起的组织反应。A7.8.2将细胞成分和组织坏死的程度划分为0~~3级。A7.8.2.1在高倍镜下观察,按炎性细胞的数量划分为0~3级,共5级。表A1炎性细胞数量划分
炎性细胞数量,个
A7. 8. 2. 2
A7. 8. 2. 3
炎性细胞数量,个
26以上
在高倍镜下观察,将组织坏死程度划分为0~3级,共5级。表A2组织坏死程度划分
无坏死
很轻微坏死
轻微坏死
采用0~~4级给出植人物样品的总毒性比率程
中等坏死
严重坏死
表A3植人物样品总毒性比率划分比
无毒性
很轻微毒性
轻微毒性
中等毒性
严重毒性
A7.8.2.4比较试样和对照样品的级别,评价试验材料的总毒性,级别<1为可接受。A7.8.3按表A1、表A2和表A3规定,观察并记录细胞成分和坏死程度,进行评价。级
动物数
植入时间(周数)
样品描述
交叉反应
组织病理切片数
细胞浸润
纤维变性
巨细胞
外物碎屑
脂肪浸润
多形核白细胞
淋巴细胞
嗜中性细胞
浆细胞
巨噬细胞
涉及区域的相应尺寸,mm
组织病理毒性比率
A8皮下植入试验
A8.1范围
YY0304—1998
表A4推荐的评价格式和等级
本试验用于评价长期接触皮下组织的材料的体内毒性。A8.2试验动物
选用年龄在80~100天的豚鼠20只,或体重180~200g的大白鼠20只。若用豚鼠,应在饮水中补充维生素C(0.8g/L)。
A8.3试样制备
按照制造厂商的使用说明书制备材料。将HA-Ti和纯Ti分别制备成直径1.3mm,长5mm的圆柱体,表面光滑,两端圆钝。经超声波清洗后,用蒸馏水洗两次。121℃30min高压蒸汽灭菌,备用。A8.4植入步骤
在每一试验动物背部,剃毛,暴露足够的面积,将剃毛区划分为4个象限,碘酒、酒精常规消毒皮肤。以外科无菌操作技术,在每个象限的皮肤上作切口,长约10mm,钝性分离达皮下组织。将试样2个对照样2个,分别放人皮下组织内,关闭切口,缝合皮肤。于植人后48h,粗略观察切口和植人区域的组织反应。并于植人后2周和12周各活杀10只动物切取植人物及其周围组织。20%中性甲醛固定石蜡包埋。制作5um厚的组织病理切片。光镜下观察植人物周围的组织改变。
A8.5组织学判断标准
组织反应
无或轻度反应
中度组织反应
重度反应
YY 0304-1998
表A5组织学判断标准
组织完好,试样周围仅见少量淋巴细胞,纤维囊壁组织完好,试样周围无或仅有少量的淋巴细胞,纤致密
试样周围有少量淋巴细胞,可见中性粒细胞、浆细胞、巨噬细胞,偶见异物巨细胞
组织反应清楚,可见嗜中性白细胞和淋巴细胞聚集,结构改变。可见小血管和纤维母细胞增生,开始形成疏松的纤维囊腔
A8.6结果评价
维囊壁稳定,无增厚趋势
可见一些慢性炎细胞、淋巴细胞、浆细胞,偶见异物巨细胞,可见纤维母细胞、纤维细胞与胶原纤维,已形成纤维囊腔结构
组织反应严重,可见淋巴细胞浆细胞、巨噬细胞聚巢,偶见异物巨细胞、嗜中性白细胞继续出现,纤维囊腔形成,增厚
A8.6.12周和12周时,出现无反应或轻度反应,表明材料是可接受的。在2周时无组织反应或轻度反应,但在12周时组织反应增加到中度或重度反应,则不能接受。A8.6.2在2周和12周时组织反应均为中度,是不能接受的,在2周时为中度反应,面在12周时变为无反应或轻度反应,是可以接受的。A8.6.3任一时间出现重度反应都是不能接受的。A8.6.4比较对照植人物和试验植人物,引起的组织反应均应符合以上三条规定。A9致敏试验
按GB11749—89中A4致敏试验。
附录B
(标准的附录)
HA涂层结晶度试验方法
结晶良好的HA粉料完全由结晶态HA组成,其X射线衍射(XRD)谱呈尖锐的特征峰。等离子喷涂过程使部分HA转变为非晶态,因而HA涂层含晶态和非晶态磷酸钙盐,其XRD谱由非晶态的弥散峰和晶态的尖锐特征峰组成。结晶良好的HA粉末和等离子喷涂HA 涂层的XRD谱如图 6 所示。HA粉末可视为完全由结晶态组成,其结晶度为100%。设HA粉末XRD谱中20=30°~35°范围内特征峰下方所围面积为R,HA涂层XRD谱中结晶态特征峰所围面积为Rc,则HA涂层结晶度为:C
用相同测试条件分别记录等离子喷涂用HA粉末和HA涂层试样的XRD谱,计算出R。和R,按式(B1)计算出结晶度C。
YY0304-1998
图B1HA粉a)和HA涂层b)的XRD谱
(标准的附录)
HA涂屡-钛基抗拉强度试验方法
试样和加载装置如图C1所示,试样用钛加工,其余部分可用不锈钢加工制作。试样的HA涂层和拉伸加载装置的端面用粘结剂粘结在一起,待粘结剂固化后,试样和加载装置起在经鉴定合格的材料试验机上进行拉伸试验。加载速度1mm/min,直至试样和加载装置扯离为止,记下扯离时的最大荷载,该荷载除以试样端面积即为HA涂层和钛基间的抗拉强度。每次测试样5只,其算术平均值应符合4.2.3规定。
粘结剂
加载装置
羟基磷灰石涂层
图C1粘结强度测试用试样和加载装置抗拉强度测试中,粘结剂类型对测试结果有明显影响,应选择本身内聚强度和粘结强度均大于涂层-钛基体粘结强度的粘结剂,否则测试值可能偏小。还应注意选择对涂层渗透性较小的较粘稠的粘结剂,162
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
等离子喷涂羟基磷灰石涂层-钛基牙种植体是由纯钛基体和其表面的羟基磷灰石涂层构成。本标准对于羟基磷灰石涂层性能指标和检测方法,主要参照美国食品和药品管理局(FDA)1992年11月11日发布的《FDA磷酸钙(Ca-P)涂层矫形种植体和骨内种植体申请认可指南》制定;对于制作基体的钛和钛合金性能指标和检测方法,则采用GB3620.2-94《钛和钛合金加工产品化学成分及成分允许偏差》中关于TA2、TA3和TC4的规定,此规定基本符合美国试验和材料学会ASTMF67:1989(1994年重新认可版本)《外科植人用钛的技术规范标准》,ASTM1341:1992《外科植人用钛丝的技术规范标准》和F136《外科植人用缎造6A1-4VELI钛合金技术规范》;对于材料的生物学评价项目选取,按YY0268一1995《口腔材料生物学评价第1单元:口腔材料生物性能评价导则》规定,生物学试验方法尽可能采用国家标准和行业标准,见附录A。A7骨植人试验参照ASTMF981:1986,《用于外科植人的无孔生物材料相容性评价(有关材料对肌肉和骨骼的作用)的实施标准》进行。HA涂层-钛基抗拉强度试验方法采用ASTMF1501:1994《磷酸钙涂层抗拉强度测试方法》,见附录C。临床应用的牙种植体具有多种形态和结构,本标准不可能对其分别作出具体规定,仅列出几种主要形态牙种植体的几何尺寸精度要求。等离子喷涂羟基磷灰石涂层-钛基牙种植体的生物学性能,不仅与材料系统有关,而且与其形态和结构设计密切相关。任何形态和结构未获市场准人的牙种植体,都应进行动物和临床试验,临床跟踪考察不得少于三年。不论牙种植体采用何种形态和结构,所有等离子喷涂羟基磷灰石涂层-钛基牙种植体都必须满足本标准规定的技术要求本标准的附录A、附录B、附录C和附录D均是标准的附录。本标准由国家医药管理局提出。本标准由全国口腔材料和器械设备标准化技术委员会归口。本标准起草单位:四川大学生物材料工程研究中心。本标准主要起草人:陈继镛、张兴栋、刘晓光、朱蔚精。151
1范围
中华人民共和国医药行业标准
等离子喷涂
羟基磷灰石涂层-钛基牙种植体
Plasma sprayed
hydroxyapatite coated titanium dental implantYY 0304-1998
本标准规定了等离子喷涂羟基磷灰石涂层-钛基牙种植体的技术要求、试验方法、产品分类、抽样、标志、标签、包装、运输及贮存等要求。本标准适用于牙缺失后颌骨内植入的等离子喷涂的羟基磷灰石涂层-钛基牙种植体。2引用标准
下列标准所包含的条文,通过在本标准中引用而构成本标准的条文。本标准出版时,所示版本均为有效。所有标准都会被修订,使用本标准的各方应探讨使用下列标准最新版本的可能性。包装储运图示标志
GB 191—901
逐批检查计数抽样程序及抽样表(适用于连续批的检查)GB 2828--87
GB 2829-87
周期检查计数抽样程序及抽样表(适用于生产过程稳定性的检查)GB3620.1-—94钛及钛合金牌号和化学成分钛及钛合金加工产品化学成分及成分允许偏差GB 3620. 2--94
GB 4698—1996
钛和钛合金化学分析方法
3化学试剂火焰原子吸收光谱法通则GB 9723—88
GB 10724—89
GB 11749--89
无火焰(石墨炉)原子吸收光谱法通则化学试剂
牙科复合树脂充填材料
YY/T0127.1-—93口腔材料生物试验方法溶血试验
YY/T 0127.2—93
YY/T 0244--1996
YY/T 0279--1995
静脉注射急性全身毒性试验
口腔材料生物试验方法
口腔材料生物试验方法
经口途径
短期全身毒性试验
口腔粘膜刺激试验
口腔材料生物试验方法
YY0268—1995口腔材料生物学评价第1单元:口腔材料生物性能评价导则中华人民共和国药典(1995年版)3定义
本标准采用下列定义。
3.1牙种植体dental implants
一类植入牙床组织内,用以支持义齿或固定松动牙的中间修复体。它可以根据需要做成圆柱状、叶片状和螺旋状等多种形态,植人粘膜内、骨内、骨膜下、根管内等牙床中不的部位。牙种植体可以由金属、陶瓷、聚合物或天然物质等不同材料所构成或由前述材料复合而成。国家医药管理局1998-04-08批准152
1998-10-01实施
YY0304—1998
3.2羟基磷灰石涂层hydroxyapatite coating利用热喷涂、沉积或烧结等不同方法,在金属、陶瓷或其他材料基体表面上形成的羟基磷灰石(HA)薄层。
3.3等离子喷涂plasma spraying热喷涂工艺的一种,是使用非转移型电弧作为热源使气体离子化,从而产生高达10000℃以上的高温,使通过喷枪送人等离子焰的喷涂材料粉料熔融或表面熔融并高速喷射到基体表面上形成涂层的方法。
3.4粘结强度adhesive strength涂层和基体间单位面积粘着力的大小。根据测试时外加载荷方向是垂直或平行于涂层-基体界面,粘结强度又可分为抗拉强度(tensile strength)和剪切强度(shear strength)。3.5HA涂层结晶度crystallinityHA涂层通常都同时包含结晶相和非晶相,HA涂层中结晶相所占百分比称为结晶度。4要求
4.1几何尺寸精度
等离子喷涂羟基磷灰石涂层-钛基牙种植体,是由植入牙槽骨内的根部及用以装设义齿的冠桩所构成。按其形态可分为圆柱状、叶片状和螺旋状等多种类型,每一类型又可按结构分为冠桩不可拆卸和冠桩可拆卸两种类型。临床使用的种植体形态和结构种类很多,其典型形态和结构如图1、图2和图3所示。通常是植入牙槽骨内的根部表面为羟基磷灰石涂层覆盖,以促进种植体和周围骨组织间的结合。对各种类型的种植体几何尺寸精度要求如下。4.1. 1圆柱状牙种植体(图1)
根部长度L,和直径D均可根据需要设计成不同尺寸,根部长度L,的极限偏差为土0.2mm,根部直径D,的极限偏差为土0.1mm。
4.1.2叶片状牙种植体(图2)
叶片状牙种植体形态和尺寸种类很多,图2所示为二个冠桩的一段式叶片状牙种植体,植入骨内的根部长度L:和宽度L的极限偏差为士0.4mm,肩部厚度3的极限偏差为士0.2mm。4.1.3螺旋状牙种植体(图3)
图3所示为一段式螺旋状牙种植体,其螺纹顶径D的极限偏差为士0.2mm,根部长度L的极限偏差为士0.4mm。
4.1.4螺纹应给出螺纹代号和螺纹公差带代号,其加工精度和公差带规定应保证冠桩可拆卸式种植体的根部和冠桩连结螺纹相互配合良好4.2物理化学性能
4.2.1外观
牙种植体未涂层的钛表面应无裂纹、无毛刺和划痕等机械加工所致的宏观缺陷,两段式种植体的根部和冠桩对中和配合应良好,配合面间无明显可见的间隙和偏移。羟基磷灰石涂层为灰白色多孔薄层,涂层表面色泽均勾并严密复盖钛基体,不得有斑点或裂纹。4.2.2化学组成
4.2.2.1HA涂层的化学组成
4.2.2.1.1涂层中HA含量和结晶度HA含量≥90%,HA结晶度≥62%。4.2.2.1.2杂质元素含量极限
图1圆柱体牙种植体
YY 0304--1998
图2叶片状牙种植体
图3螺旋状牙种植体
砷≤3mg/kg,镉≤5mg/kg,汞≤5mg/kg,铅≤30mg/kg重金属元素总量(以铅计)≤50mg/kg。4.2.2.2钛材化学组成
应符合GB3620.2中关于TA2、TA3或TC4的规定。4.2.3HA涂层和钛基体粘结(抗拉)强度抗拉强度≥30MPa。
4.3生物学性能
4.3.1溶血试验
溶血率≤5%。
4.3.2细胞毒性试验
应为0~1级。
4.3.3静脉注射急性全身毒性试验无毒性。
4.3.4短期全身毒性试验:经口途径无毒性。
4.3.5口腔粘膜刺激试验(钛材)154
无刺激。
4.3.6Ames试验
诱变试验阴性。
4.3.7骨植入应用试验
总毒性比率为1~0级(≤1级)。4.3.8皮下植入试验
埋植12周,无反应或轻度反应。4.3.9致敏试验
无过敏反应。
5试验方法
5.1牙种植体几何尺寸
YY 0304—1998
几何尺寸精度用千分尺或千分表测量,精度:二级,0.01mm士0.001mm。连接螺纹加工精度用螺纹塞规或螺纹环规检验。使用的塞规和环规公差带应与螺纹公差带一致。5.2物理化学性能Www.vV99.net
5.2.1外观
目测法。
5.2.2化学组成
5.2.2.1羟基磷灰石涂层的化学成分5.2.2.1.1涂层HA含量和结晶度
用陪片进行测试,陪片的基底为12mm×12mm×1.5mm的钛片,共三片,按与同批号产品相同的工艺条件在钛片上制作HA涂层,然后记录陪片的X射线衍射谱(XRD谱),HA含量计算按附录D进行。结晶度计算方法见附录B。
5.2.2.1.2HA涂层微量杂质含量和重金属元素总量用与同批号产品相同的喷涂工艺,在清洁钛片上多次重复喷涂HA厚涂层。将厚涂层从钛片上剥离下来进行测试。砷含量测试按《中华人民共和国药典》(1995年版)碑盐检查法;和铅含量测试按GB10724进行;汞含量测试按GB9723进行:重金属元素总量测试按《中华人民共和国药典》(1995年版)附录中重金属检验法进行。
5.2.2.2钛材化学组成
按GB4698规定进行。
5.2.3涂层和钛基体界面抗拉强度抗拉强度检测按附录C进行。
5.3生物学试验
见附录A《等离子喷涂HA-Ti牙种植体生物学试验方法》。6检验规则
6.1每一批产品均应经生产厂技术检验部门进行检查,合格后方可提交验收。6.2产品必须按批号成批提交检查。检查分为逐批检查和周期检查。6.3逐批检查
6.3.1逐批检查按GB2828的规定进行。6.3.2抽样方案类型
采用一次抽样。抽样方案严格性按正常检查抽样方案进行,检查水平为I,缺陷分类、检查项目和AQL(合格质量水平)按表1的规定。采取随机抽样方式抽取被检查的样本。155
缺陷分类
检查项目
6.4周期检查
6.4.1在下列情况下应进行周期检查:a)产品初次投产前;
b)间隔1年以上再投产时;
YY 0304--1998
逐批检查
4.1.1,4.1.4,4.2.1
c)设计、工艺或生产设备有重大改变时。轻
4.1.2,4.1.3
6.4.2对表1所列检查项目,周期检查前应先进行逐批检查,从逐批检查合格的批中抽取样本进行周期检查,周期检查按GB2829进行,采用一次抽样方案,从连续5批产品中,每批随机抽取4个试样,共20个试样组成样本,判定数组和不合格质量水平(RQL)见表2。6.4.3周期检查合格,必须是本周期所有检查项目都合格,否则就认为周期检查不合格。表 2周期检查
检查项目
4.2.2.1.1
4.2.2.1.2
检查周期
6.4.1规定情况
1)6.4.1规定情况;
2)更换喷涂用HA粉批号时
1)6.4.1规定情况;
2)每年一次
1)6.4.1规定情况;
2)每六个月一次
每批钛材购进时
6.4.1规定情况
7标志、标签、包装、运输、贮存判定数组或合格标准
n= 20[A=1,Re= 2]
n- 3A = 0,R --1]
杂质元素含量符合4.2.2.1.2规定算术平均值符合4.2.3规定
符合GB3620.2的有关规定
符合4,3规定
7.1牙种植体必须包装在密封的容器中。容器材料应无毒,不污染和影响牙种植体性能,包装容器还应具有正常搬运或储存期间不损坏、不破裂的性能。7.2内包装上应注明规格、型号、商标和批号。7.3中包装为硬塑料或其他无毒硬质盒。中包装上应注明制造厂名称、商标和地址、产品名称、型号、数量和批号。
7.4每一中包装盒内应附有牙种植体使用说明书,使用说明书应按国家有关规定编写,至少应有下列内容:
a)牙种植体的材质类型;
b)牙种植体消毒方法;
c)临床使用简要说明;
d)牙种植体贮存保管注意事项,YY 0304-1998
e)牙种植体使用过程中可能出现的意外及应采取的措施。5运输包装采用木箱,封装后的成品置于木箱内,内盖用软纸或泡沫塑料填塞。木箱上标明防潮、防7.5
震、远离有害物质等字样或标志。157
A1溶血试验
按 YY/T0127.1。
YY 0304-1998
附录A
(标雅的附录)
等离子喷涂HA-Ti牙种植体生物学试验方法A2细胞毒性试验(分子过滤法)按GB11749--89中 A2。
A3 静脉注射急性全身毒性试验
按 YY/T 0127. 2。
A4短期全身毒性试验:经口途径按 YY/T 0244
A5口腔粘膜刺激试验(钛材)
按 YY/T 0279。
A6 Ames 试验
按GB11749—89中A3,试样为材料浸提液。A7骨植入试验
A7.1范围
本试验适用于外科植入,无吸收的生物材料的组织反应,适用于评价在人体骨骼内停留超过30天,且不被吸收的材料。
A7.2植人试样的制备
A7.2.1将受试材料制备成直径2mm,长6mm圆柱体,表面光洁,同时制备直径2mm,长6mm阴性对照试样。
A7.2.2试样与对照样品经自来水冲洗,超声波清洗两次,0.9%的氧化钠(NaCI)清洗两次,每次约1min,高压蒸汽灭菌。
A7.2.3植入样品的清洁、包装、消毒方式应与产品临床应用一致。A7.3试验动物
选用体重2~2.5kg大白兔。
A7.4植人期间
以相间的外科手术将所有的植人样品,分别植入每只动物,以便使植人期间的组织反应相一致。每时间至少4只大白兔。
A7.5植人步骤
A7.5.1采用灭菌操作技术,暴露动物股骨外侧骨皮质,用符合要求的设备和技术,以2000~3000r/min的速度,在股骨外侧骨皮质上钻三个孔(直径2mm),分别用手指或器械将植人样品压人洞内,每条股骨植人试样2个,对照样1个,然后缝合封闭创口。158
A7.6植入物的取出和动物处死
YY 0304—1998
A7.6、1于植人后1、2、4、8、12、26和52周,动脉放血处死动物,每次4只。A7.6.2观察植人物及其周围组织,记录肉眼所见的改变。A7.6.3将植入物及其周围的骨组织-起取下来,在切取的组织样品中,至少要包含5mm厚的植入物周围组织。
A7.7组织学样品制备
A7.7.1自每一植人部位制备组织块。A7.7.2将组织块置20%甲醛溶液中固定,制备成组织病理切片,切组织片时,应由端到另端同时记录植人样品周围组织的肉眼观察所见。A7.7.3如果需要特殊染色,应另外制备组织块或切片。A7.8组织病理观察
A7.8.1观察试样周围组织的病理反应,并与对照样品周围的组织反应相比较。观察癜痕厚度,炎性细胞或其他种类的细胞以及在试验条件下确实由材料引起的组织反应。A7.8.2将细胞成分和组织坏死的程度划分为0~~3级。A7.8.2.1在高倍镜下观察,按炎性细胞的数量划分为0~3级,共5级。表A1炎性细胞数量划分
炎性细胞数量,个
A7. 8. 2. 2
A7. 8. 2. 3
炎性细胞数量,个
26以上
在高倍镜下观察,将组织坏死程度划分为0~3级,共5级。表A2组织坏死程度划分
无坏死
很轻微坏死
轻微坏死
采用0~~4级给出植人物样品的总毒性比率程
中等坏死
严重坏死
表A3植人物样品总毒性比率划分比
无毒性
很轻微毒性
轻微毒性
中等毒性
严重毒性
A7.8.2.4比较试样和对照样品的级别,评价试验材料的总毒性,级别<1为可接受。A7.8.3按表A1、表A2和表A3规定,观察并记录细胞成分和坏死程度,进行评价。级
动物数
植入时间(周数)
样品描述
交叉反应
组织病理切片数
细胞浸润
纤维变性
巨细胞
外物碎屑
脂肪浸润
多形核白细胞
淋巴细胞
嗜中性细胞
浆细胞
巨噬细胞
涉及区域的相应尺寸,mm
组织病理毒性比率
A8皮下植入试验
A8.1范围
YY0304—1998
表A4推荐的评价格式和等级
本试验用于评价长期接触皮下组织的材料的体内毒性。A8.2试验动物
选用年龄在80~100天的豚鼠20只,或体重180~200g的大白鼠20只。若用豚鼠,应在饮水中补充维生素C(0.8g/L)。
A8.3试样制备
按照制造厂商的使用说明书制备材料。将HA-Ti和纯Ti分别制备成直径1.3mm,长5mm的圆柱体,表面光滑,两端圆钝。经超声波清洗后,用蒸馏水洗两次。121℃30min高压蒸汽灭菌,备用。A8.4植入步骤
在每一试验动物背部,剃毛,暴露足够的面积,将剃毛区划分为4个象限,碘酒、酒精常规消毒皮肤。以外科无菌操作技术,在每个象限的皮肤上作切口,长约10mm,钝性分离达皮下组织。将试样2个对照样2个,分别放人皮下组织内,关闭切口,缝合皮肤。于植人后48h,粗略观察切口和植人区域的组织反应。并于植人后2周和12周各活杀10只动物切取植人物及其周围组织。20%中性甲醛固定石蜡包埋。制作5um厚的组织病理切片。光镜下观察植人物周围的组织改变。
A8.5组织学判断标准
组织反应
无或轻度反应
中度组织反应
重度反应
YY 0304-1998
表A5组织学判断标准
组织完好,试样周围仅见少量淋巴细胞,纤维囊壁组织完好,试样周围无或仅有少量的淋巴细胞,纤致密
试样周围有少量淋巴细胞,可见中性粒细胞、浆细胞、巨噬细胞,偶见异物巨细胞
组织反应清楚,可见嗜中性白细胞和淋巴细胞聚集,结构改变。可见小血管和纤维母细胞增生,开始形成疏松的纤维囊腔
A8.6结果评价
维囊壁稳定,无增厚趋势
可见一些慢性炎细胞、淋巴细胞、浆细胞,偶见异物巨细胞,可见纤维母细胞、纤维细胞与胶原纤维,已形成纤维囊腔结构
组织反应严重,可见淋巴细胞浆细胞、巨噬细胞聚巢,偶见异物巨细胞、嗜中性白细胞继续出现,纤维囊腔形成,增厚
A8.6.12周和12周时,出现无反应或轻度反应,表明材料是可接受的。在2周时无组织反应或轻度反应,但在12周时组织反应增加到中度或重度反应,则不能接受。A8.6.2在2周和12周时组织反应均为中度,是不能接受的,在2周时为中度反应,面在12周时变为无反应或轻度反应,是可以接受的。A8.6.3任一时间出现重度反应都是不能接受的。A8.6.4比较对照植人物和试验植人物,引起的组织反应均应符合以上三条规定。A9致敏试验
按GB11749—89中A4致敏试验。
附录B
(标准的附录)
HA涂层结晶度试验方法
结晶良好的HA粉料完全由结晶态HA组成,其X射线衍射(XRD)谱呈尖锐的特征峰。等离子喷涂过程使部分HA转变为非晶态,因而HA涂层含晶态和非晶态磷酸钙盐,其XRD谱由非晶态的弥散峰和晶态的尖锐特征峰组成。结晶良好的HA粉末和等离子喷涂HA 涂层的XRD谱如图 6 所示。HA粉末可视为完全由结晶态组成,其结晶度为100%。设HA粉末XRD谱中20=30°~35°范围内特征峰下方所围面积为R,HA涂层XRD谱中结晶态特征峰所围面积为Rc,则HA涂层结晶度为:C
用相同测试条件分别记录等离子喷涂用HA粉末和HA涂层试样的XRD谱,计算出R。和R,按式(B1)计算出结晶度C。
YY0304-1998
图B1HA粉a)和HA涂层b)的XRD谱
(标准的附录)
HA涂屡-钛基抗拉强度试验方法
试样和加载装置如图C1所示,试样用钛加工,其余部分可用不锈钢加工制作。试样的HA涂层和拉伸加载装置的端面用粘结剂粘结在一起,待粘结剂固化后,试样和加载装置起在经鉴定合格的材料试验机上进行拉伸试验。加载速度1mm/min,直至试样和加载装置扯离为止,记下扯离时的最大荷载,该荷载除以试样端面积即为HA涂层和钛基间的抗拉强度。每次测试样5只,其算术平均值应符合4.2.3规定。
粘结剂
加载装置
羟基磷灰石涂层
图C1粘结强度测试用试样和加载装置抗拉强度测试中,粘结剂类型对测试结果有明显影响,应选择本身内聚强度和粘结强度均大于涂层-钛基体粘结强度的粘结剂,否则测试值可能偏小。还应注意选择对涂层渗透性较小的较粘稠的粘结剂,162
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。