如图是实验室常用气体制备装置,据图回答问题:(1)用A装置制取氧气的化学方程式是.选择D装置收集氧气是因为.将带火星的木炭深入盛有氧气的集气瓶中,木炭剧烈燃烧,发出白光,说明氧气能,该反应的化学方程式为.(2)实验室制取氨气:Ca(OH)2(固)+2NH4Cl(固) △ .
2019-04-20
如图是实验室常用气体制备装置,据图回答问题:
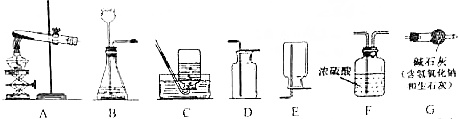
(1)用A装置制取氧气的化学方程式是___.选择D装置收集氧气是因为___.将带火星的木炭深入盛有氧气的集气瓶中,木炭剧烈燃烧,发出白光,说明氧气能___,该反应的化学方程式为___.
(2)实验室制取氨气:Ca(OH)2(固)+2NH4Cl(固)
CaCl2(固)+2H2O+2NH3↑,要制取并收集干燥的氨气,所选装置正确的连接顺序是___→___→___(填字母代号).
(3)为探究氨气的性质,按如图装置进行实验.观察到黑色粉末变红,白色无水硫酸铜变蓝,同时反应中还有一种气体单质生成.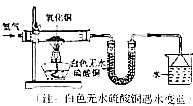
【查阅资料】Cu2O是红色,易与稀硫酸反应:Cu2O+H2SO4═CuSO4+Cu+H2O.
【提出问题】得到的红色物质是什么?
【猜想】①是Cu;②是Cu2O;③是___.
若猜想①成立,玻璃管中发生反应的化学方程式为___,说明NH3具有___性.
【设计实验】请你设计一个简单的实验来验证红色物质中是否存在Cu2O:___.

(1)用A装置制取氧气的化学方程式是___.选择D装置收集氧气是因为___.将带火星的木炭深入盛有氧气的集气瓶中,木炭剧烈燃烧,发出白光,说明氧气能___,该反应的化学方程式为___.
(2)实验室制取氨气:Ca(OH)2(固)+2NH4Cl(固)
| ||
(3)为探究氨气的性质,按如图装置进行实验.观察到黑色粉末变红,白色无水硫酸铜变蓝,同时反应中还有一种气体单质生成.

【查阅资料】Cu2O是红色,易与稀硫酸反应:Cu2O+H2SO4═CuSO4+Cu+H2O.
【提出问题】得到的红色物质是什么?
【猜想】①是Cu;②是Cu2O;③是___.
若猜想①成立,玻璃管中发生反应的化学方程式为___,说明NH3具有___性.
【设计实验】请你设计一个简单的实验来验证红色物质中是否存在Cu2O:___.