在化学及其八领域中,都存在着平衡的问题,平衡移动原理也是一条普遍适用的规律,请运用有关知识回答下列问题.(1)在容积不同的密闭容器内,分别充入同量的52和f2,在不同温度下,任其发生反应52+3f2⇌25f3,并分别在t秒时测定其中5f3的体积分数,绘图如图所示:①A,B,C,D,4五点中,尚未达到化学平衡状态的点是.②此可逆反应的正反应是反应.(放热、吸热)(2)将52和f2混和,使其在一定条件下发生反应并达到平衡.根据表中数据回答有关问题:物质52f25f3起始浓度(摩/升)a60转化浓度(摩/升)b
2019-11-24
在化学及其八领域中,都存在着平衡的问题,平衡移动原理也是一条普遍适用的规律,请运用有关知识回答下列问题.
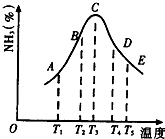 (1)在容积不同的密闭容器内,分别充入同量的52和f2,在不同温度下,任其发生反应52+3f2⇌25f3,并分别在t秒时测定其中5f3的体积分数,绘图如图所示:
(1)在容积不同的密闭容器内,分别充入同量的52和f2,在不同温度下,任其发生反应52+3f2⇌25f3,并分别在t秒时测定其中5f3的体积分数,绘图如图所示:
①A,B,C,D,4五点中,尚未达到化学平衡状态的点是______.
②此可逆反应的正反应是______反应.(放热、吸热)
(2)将52和f2混和,使其在一定条件下发生反应并达到平衡.根据表中数据回答有关问题:
①表中a=______,4=______.
②若反应经3分钟达到平衡,则反应速度v(52)=______.
③氮气的转化率是______.
④该体系的起始状态和平衡状态的压强比(体积、温度不变)是______.
 (1)在容积不同的密闭容器内,分别充入同量的52和f2,在不同温度下,任其发生反应52+3f2⇌25f3,并分别在t秒时测定其中5f3的体积分数,绘图如图所示:
(1)在容积不同的密闭容器内,分别充入同量的52和f2,在不同温度下,任其发生反应52+3f2⇌25f3,并分别在t秒时测定其中5f3的体积分数,绘图如图所示:①A,B,C,D,4五点中,尚未达到化学平衡状态的点是______.
②此可逆反应的正反应是______反应.(放热、吸热)
(2)将52和f2混和,使其在一定条件下发生反应并达到平衡.根据表中数据回答有关问题:
| 物质 | 52 | f2 | 5f3 |
| 起始浓度(摩/升) | a | 6 | 0 |
| 转化浓度(摩/升) | b | c | d |
| 平衡浓度(摩/升) | 1 | 4 | 3 |
②若反应经3分钟达到平衡,则反应速度v(52)=______.
③氮气的转化率是______.
④该体系的起始状态和平衡状态的压强比(体积、温度不变)是______.