某实验小组用下列装置进行乙醇的实验,试回答下列问题:(1)A中发生反应的化学方程式为:2H2O2 MnO2 . 2H2O+O2↑2H2O2 MnO2 . 2H2O+O2↑,还可以用 代替 MnO2的作用(2)实验过程中D处铜丝网有红色和黑色交替出现的现象,请用化学方程式解释原因.现象①:红色变黑色:2Cu+O2 △ . 2CuO2Cu+O2 △&nbs
2019-05-30
某实验小组用下列装置进行乙醇的实验,试回答下列问题:
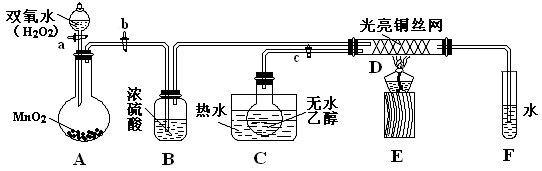
(1)A中发生反应的化学方程式为:,还可以用______ 代替 MnO2的作用
(2)实验过程中D处铜丝网有红色和黑色交替出现的现象,请用化学方程式解释原因.
现象①:红色变黑色:
现象②:黑色变红色:CH
3CH
2OH+CuO
CH
3CHO+Cu+H
2O
CH
3CH
2OH+CuO
CH
3CHO+Cu+H
2O
(3)在F装置中,由于产物速率不易控制,有可能造成倒吸,所以F装置可改用______装置(填字母).

(4)实验室可对E部分采取合理的操作方法以防止安全隐患,请对此提出你的意见:______.
优质解答
(1)双氧水在二氧化锰的催化作用下能迅速分解生成水和氧气,2H2O22H2O+O2↑;除二氧化锰能加快双氧水的分解外,氯化铁也能加快双氧水的分解;
故答案为:2H2O22H2O+O2↑;FeCl3;
(2)红色的铜丝在空气中加热能生成黑色的氧化铜2Cu+O22CuO;黑色的氧化铜能和乙醇反应生成乙醛、铜和水CH3CH2OH+CuOCH3CHO+Cu+H2O,该反应中乙醇失电子作还原剂,发生氧化反应,
故答案为:2Cu+O22CuO;CH3CH2OH+CuOCH3CHO+Cu+H2O;氧化反应;
(3)在加热条件下,未反应的乙醇蒸汽和生成物乙醛蒸汽都极易溶于水,所以可用水吸收乙醇和乙醛蒸汽;乙醇和乙醛蒸汽的密度大于空气的密度,所以可用向上排空气法收集气体,a装置即使有液体进入集气瓶因为进气管较短,溶液不能进入进气管,故可选a;b装置是倒置的干燥管,即使溶液进入干燥管,但干燥管有缓冲作用,故可选b;c装置有溶液进入集气瓶后,因为进气管较长,进入的液体有可能进入进气口,故c错误.
故答案为:ab;
(4)乙醇和氧化铜的反应是放热反应,该反应引发后,不需加热即可进行,所以可以采用在反应开始后撤去E处酒精灯或根本不用E处酒精灯,反应开始时把红热的铜丝直接放入E装置的操作方式,
故答案为:可以采用在反应开始后撤去E处酒精灯或根本不用E处酒精灯,反应开始时把红热的铜丝直接放入E装置的操作方式.
(1)双氧水在二氧化锰的催化作用下能迅速分解生成水和氧气,2H2O22H2O+O2↑;除二氧化锰能加快双氧水的分解外,氯化铁也能加快双氧水的分解;
故答案为:2H2O22H2O+O2↑;FeCl3;
(2)红色的铜丝在空气中加热能生成黑色的氧化铜2Cu+O22CuO;黑色的氧化铜能和乙醇反应生成乙醛、铜和水CH3CH2OH+CuOCH3CHO+Cu+H2O,该反应中乙醇失电子作还原剂,发生氧化反应,
故答案为:2Cu+O22CuO;CH3CH2OH+CuOCH3CHO+Cu+H2O;氧化反应;
(3)在加热条件下,未反应的乙醇蒸汽和生成物乙醛蒸汽都极易溶于水,所以可用水吸收乙醇和乙醛蒸汽;乙醇和乙醛蒸汽的密度大于空气的密度,所以可用向上排空气法收集气体,a装置即使有液体进入集气瓶因为进气管较短,溶液不能进入进气管,故可选a;b装置是倒置的干燥管,即使溶液进入干燥管,但干燥管有缓冲作用,故可选b;c装置有溶液进入集气瓶后,因为进气管较长,进入的液体有可能进入进气口,故c错误.
故答案为:ab;
(4)乙醇和氧化铜的反应是放热反应,该反应引发后,不需加热即可进行,所以可以采用在反应开始后撤去E处酒精灯或根本不用E处酒精灯,反应开始时把红热的铜丝直接放入E装置的操作方式,
故答案为:可以采用在反应开始后撤去E处酒精灯或根本不用E处酒精灯,反应开始时把红热的铜丝直接放入E装置的操作方式.



