磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:请回答:(1)A的组成元素为(用化学符号表示),化学式为;(2)C溶液可溶解铜片,例举该反应的一个实际应用;(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518g•L-1),该气体分子的电子式为,写出该反应的离子方程式;(4)写出F→G反应的化学方程式,设计实验方案探究溶液G中的主要微粒(不考虑H2O,H+,K+,I-).
2019-04-20
磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
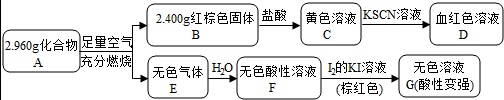
请回答:
(1)A的组成元素为___(用化学符号表示),化学式为___;
(2)C溶液可溶解铜片,例举该反应的一个实际应用___;
(3)已知化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518g•L-1),该气体分子的电子式为___,写出该反应的离子方程式___;
(4)写出F→G反应的化学方程式,设计实验方案探究溶液G中的主要微粒(不考虑H2O,H+,K+,I-)___.
优质解答
C加入KSCN,D为血红色溶液,可知C为FeCl3,D为Fe(SCN)3等,可知B为Fe2O3,且n(Fe2O3)==0.015mol,n(Fe)=0.03mol,m(Fe)=0.03mol×56g/mol=1.68g,A燃烧生成的无色气体E溶液水得到酸性溶液,加入碘的KI溶液,得到无色溶液,说明碘可氧化E的水溶液,E应为SO2,F为H2SO3,G含有和H2SO4和HI,可知A含有Fe、S元素,且m(S)=2.96g-1.68g=1.28g,n(S)==0.04mol,可知n(Fe):n(S)=3:4,应为Fe3S4,
(1)由以上分析可知,A组成元素为Fe、S,为Fe3S4,故答案为:Fe、S;Fe3S4;
(2)铁离子具有强氧化性,可氧化铜,常用于刻饰铜线路板,故答案为:刻饰铜线路板;
(3)化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518g•L-1),淡黄色不溶物为S,气体的相对分子质量为1.518×22.4L=34,为H2S气体,电子式为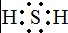 ,反应的离子方程式为Fe3S4+6H++=3Fe2++S+3H2S↑,
,反应的离子方程式为Fe3S4+6H++=3Fe2++S+3H2S↑,
故答案为: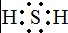 ;Fe3S4+6H++=3Fe2++S+3H2S↑;
;Fe3S4+6H++=3Fe2++S+3H2S↑;
(4)F→G反应的化学方程式为H2SO3+I2+H2O=H2SO4+2HI,溶液G中的主要微粒(不考虑H2O,H+,K+,I-) 为SO42-和H2SO3,可先检验SO42-,后检验有H2SO3,具体操作为:取溶液G,加入过量BaCl2溶液,若产生白色沉淀,则有SO42-;过滤后取滤液,滴加H2O2溶液,若再产生白色沉淀,则有H2SO3.
故答案为:H2SO3+I2+H2O=H2SO4+2HI;取溶液G,加入过量BaCl2溶液,若产生白色沉淀,则有SO42-;过滤后取滤液,滴加H2O2溶液,若再产生白色沉淀,则有H2SO3.
C加入KSCN,D为血红色溶液,可知C为FeCl3,D为Fe(SCN)3等,可知B为Fe2O3,且n(Fe2O3)==0.015mol,n(Fe)=0.03mol,m(Fe)=0.03mol×56g/mol=1.68g,A燃烧生成的无色气体E溶液水得到酸性溶液,加入碘的KI溶液,得到无色溶液,说明碘可氧化E的水溶液,E应为SO2,F为H2SO3,G含有和H2SO4和HI,可知A含有Fe、S元素,且m(S)=2.96g-1.68g=1.28g,n(S)==0.04mol,可知n(Fe):n(S)=3:4,应为Fe3S4,
(1)由以上分析可知,A组成元素为Fe、S,为Fe3S4,故答案为:Fe、S;Fe3S4;
(2)铁离子具有强氧化性,可氧化铜,常用于刻饰铜线路板,故答案为:刻饰铜线路板;
(3)化合物A能与稀硫酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518g•L-1),淡黄色不溶物为S,气体的相对分子质量为1.518×22.4L=34,为H2S气体,电子式为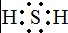 ,反应的离子方程式为Fe3S4+6H++=3Fe2++S+3H2S↑,
,反应的离子方程式为Fe3S4+6H++=3Fe2++S+3H2S↑,
故答案为: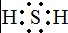 ;Fe3S4+6H++=3Fe2++S+3H2S↑;
;Fe3S4+6H++=3Fe2++S+3H2S↑;
(4)F→G反应的化学方程式为H2SO3+I2+H2O=H2SO4+2HI,溶液G中的主要微粒(不考虑H2O,H+,K+,I-) 为SO42-和H2SO3,可先检验SO42-,后检验有H2SO3,具体操作为:取溶液G,加入过量BaCl2溶液,若产生白色沉淀,则有SO42-;过滤后取滤液,滴加H2O2溶液,若再产生白色沉淀,则有H2SO3.
故答案为:H2SO3+I2+H2O=H2SO4+2HI;取溶液G,加入过量BaCl2溶液,若产生白色沉淀,则有SO42-;过滤后取滤液,滴加H2O2溶液,若再产生白色沉淀,则有H2SO3.


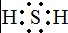 ,反应的离子方程式为Fe3S4+6H++=3Fe2++S+3H2S↑,
,反应的离子方程式为Fe3S4+6H++=3Fe2++S+3H2S↑,