某中学初三化学兴趣小组的同学利用课余时间证明铁、铜、镁的金属活动性强弱.(1)如图1,小雯的方案:(所用金属的大小、形状、质量完全相同,酸的质量相同)记录现象: 金属 铁粉 铜粉 镁粉 与酸反应的现象 气泡产生缓慢,金属逐渐溶解 无气泡产生,金属无变化 气泡产生剧烈,金属迅速溶解得出结论:(1)金属活动性由强到弱依次为.(2)小芳认为,上述方案的设计有错误之处,请改正.(3)小华认为,用如图2所示的装置及药品,也能够得出结论,x溶液中溶质的化学式为.(4)将铁粉和镁粉的混合
2019-04-20
某中学初三化学兴趣小组的同学利用课余时间证明铁、铜、镁的金属活动性强弱.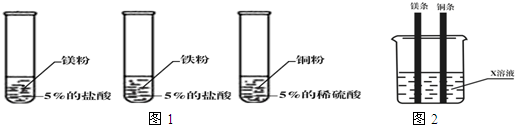
(1)如图1,小雯的方案:(所用金属的大小、形状、质量完全相同,酸的质量相同)
记录现象:
得出结论:(1)金属活动性由强到弱依次为______.
(2)小芳认为,上述方案的设计有错误之处,请改正______.
(3)小华认为,用如图2所示的装置及药品,也能够得出结论,x溶液中溶质的化学式为______.
(4)将铁粉和镁粉的混合物放入硫酸铜溶液中,反应结束后,过滤,对所得滤渣中固体的成分的判断不正确的是______(单选)
①可能有铜 ②若固体中有镁,则一定有铁
③若固体中有铁,则可能有镁 ④可能是铁、镁和铜.

(1)如图1,小雯的方案:(所用金属的大小、形状、质量完全相同,酸的质量相同)
记录现象:
| 金属 | 铁粉 | 铜粉 | 镁粉 |
| 与酸反应 的现象 | 气泡产生缓慢,金属逐渐溶解 | 无气泡产生,金属无变化 | 气泡产生剧烈,金属迅速溶解 |
(2)小芳认为,上述方案的设计有错误之处,请改正______.
(3)小华认为,用如图2所示的装置及药品,也能够得出结论,x溶液中溶质的化学式为______.
(4)将铁粉和镁粉的混合物放入硫酸铜溶液中,反应结束后,过滤,对所得滤渣中固体的成分的判断不正确的是______(单选)
①可能有铜 ②若固体中有镁,则一定有铁
③若固体中有铁,则可能有镁 ④可能是铁、镁和铜.