(10分)初中化学课上,同学们利用下列实验探究碱的化学性质: (1)A实验中反应的化学方程式为。(2)C实验中观察到的现象是。(3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。【提出问题】 废液中含有什么物质?【假设猜想】 通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有。老师问:废液中还可能有什么物质?引发了同学们热烈讨论,下面是大家的发言: 学生甲 可能有Ca(OH) 2 、NaOH 学生丙 可能有Ca(OH) 2 、CaCl 2 学生
2019-11-23
| (10分)初中化学课上,同学们利用下列实验探究碱的化学性质: 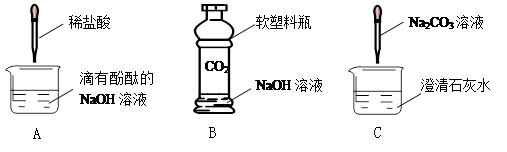 (1)A实验中反应的化学方程式为________________________________________。 (2)C实验中观察到的现象是____________________________________________。 (3)实验结束后,同学们将废液倒入同一只废液缸中,最后发现废液浑浊并显红色。 【提出问题】 废液中含有什么物质? 【假设猜想】 通过分析上述实验,同学们猜想:废液中除酚酞、碳酸钙及水以外一定含有___________。 老师问:废液中还可能有什么物质?引发了同学们热烈讨论,下面是大家的发言:
【实验验证】 同学们对可能含有的物质进行确定,取一定量的废液过滤,向滤液中逐滴加入氯化钡溶液,得到白色沉淀,红色褪去。 【结论】上述滤液中,还含有________,没有______________________。 |