优质解答
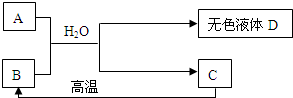
(1)由反应:钠盐A+氢氧化钙→碳酸钙+D可知,钠盐A为碳酸钠其化学式为Na2CO3;由反应碳酸钙高温分解生成二氧化碳和氧化钙,B为该反应的生成物且能与水生成氢氧化钙可知,B为氧化钙化学式为CaO;由“C为相对分子质量为100的白色不溶物”推知,C为碳酸钙其化学式为CaCO3;
故答:Na2CO3,CaO,CaCO3;
(2)D溶液为碳酸钠和氢氧化钙反应后所形成的溶液,根据反应Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,反应后溶液一定含有NaOH;其中反应物氢氧化钙由氧化钙与水反应所得,反应化学方程式为CaO+H2O═Ca(OH)2;
故答:NaOH,CaO+H2O═Ca(OH)2,Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(3)由于反应物碳酸钠或氢氧化钙可能过量,反应后溶液可能混有碳酸钠或氢氧化钙之一,所以反应后溶液的组成可能有:Na2CO3; 或Ca(OH)2;
故答:Na2CO3或 Ca(OH)2.
(1)由反应:钠盐A+氢氧化钙→碳酸钙+D可知,钠盐A为碳酸钠其化学式为Na2CO3;由反应碳酸钙高温分解生成二氧化碳和氧化钙,B为该反应的生成物且能与水生成氢氧化钙可知,B为氧化钙化学式为CaO;由“C为相对分子质量为100的白色不溶物”推知,C为碳酸钙其化学式为CaCO3;
故答:Na2CO3,CaO,CaCO3;
(2)D溶液为碳酸钠和氢氧化钙反应后所形成的溶液,根据反应Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,反应后溶液一定含有NaOH;其中反应物氢氧化钙由氧化钙与水反应所得,反应化学方程式为CaO+H2O═Ca(OH)2;
故答:NaOH,CaO+H2O═Ca(OH)2,Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(3)由于反应物碳酸钠或氢氧化钙可能过量,反应后溶液可能混有碳酸钠或氢氧化钙之一,所以反应后溶液的组成可能有:Na2CO3; 或Ca(OH)2;
故答:Na2CO3或 Ca(OH)2.