对一个化学反应的研究需要从反应条件、限度、速率、定量关系等因素进行综合分析,下列是关于化学反应原理的系列研究,请根据相关信息回答有关问题.(1)关于反应生成物的定量研究:已知反应:Br2+2Fe2+═2Br-+2Fe3+,向10mL 0.1mol•L-1的FeBr2溶液中通入0.001mol Cl2,反应后,溶液中除含有Cl-外,还一定.(填字母序号)A.含Fe2+,不含Fe3+B.含Fe3+,不含Br-C.含Fe3+,含有Br-(2)关于反应限度的研究:已知在773K、固定体积的容器
2019-04-20
对一个化学反应的研究需要从反应条件、限度、速率、定量关系等因素进行综合分析,下列是关于化学反应原理的系列研究,请根据相关信息回答有关问题.
(1)关于反应生成物的定量研究:
已知反应:Br2+2Fe2+═2Br-+2Fe3+,向10mL 0.1mol•L-1的FeBr2溶液中通入0.001mol Cl2,反应后,溶液中除含有Cl-外,还一定______.(填字母序号)
A.含Fe2+,不含Fe3+B.含Fe3+,不含Br-C.含Fe3+,含有Br-
(2)关于反应限度的研究:
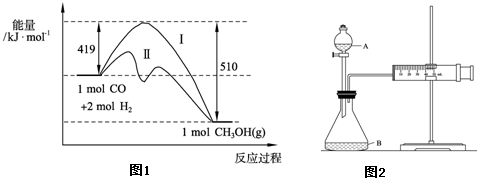
已知在773K、固定体积的容器中,反应CO(g)+2H2(g)⇌CH3OH(g)过程中能量变化如图1.曲线Ⅱ表示使用催化剂时的能量
变化.若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值.
①若按上述投料比使该反应具有工业应用价值,CO的平衡转化率最小为______;
②在容器容积不变的前提下,欲提高H2的转化率,可采取的措施(答两项即可):______、______;
(3)关于反应速率的研究:
氧化还原反应中实际上包含氧化和还原两个过程.下面是HNO3发生 的一个还原过程的反应式:NO3-+4H++3e-→NO+2H2O
①KMnO4、Na2CO3、CuO、KI四种物质中的______ (填化学式)能使上述还原过程发生.
②欲用图2装置测算硝酸被还原的速率,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定______推(计)算反应速率.

(1)关于反应生成物的定量研究:
已知反应:Br2+2Fe2+═2Br-+2Fe3+,向10mL 0.1mol•L-1的FeBr2溶液中通入0.001mol Cl2,反应后,溶液中除含有Cl-外,还一定______.(填字母序号)
A.含Fe2+,不含Fe3+B.含Fe3+,不含Br-C.含Fe3+,含有Br-
(2)关于反应限度的研究:
已知在773K、固定体积的容器中,反应CO(g)+2H2(g)⇌CH3OH(g)过程中能量变化如图1.曲线Ⅱ表示使用催化剂时的能量
变化.若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值.
①若按上述投料比使该反应具有工业应用价值,CO的平衡转化率最小为______;
②在容器容积不变的前提下,欲提高H2的转化率,可采取的措施(答两项即可):______、______;
(3)关于反应速率的研究:
氧化还原反应中实际上包含氧化和还原两个过程.下面是HNO3发生 的一个还原过程的反应式:NO3-+4H++3e-→NO+2H2O
①KMnO4、Na2CO3、CuO、KI四种物质中的______ (填化学式)能使上述还原过程发生.
②欲用图2装置测算硝酸被还原的速率,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定______推(计)算反应速率.