甲醇(CH3OH))是一种重要的有机物,有重要的应用.(1)甲醇作燃料燃烧的化学方程式为2CH3OH+3O2 点燃 . 2CO2+4H2O,该反应中化学能主要转化为,该反应的氧化剂是.(2)将甲醇和氧气分别通入如图装置中形成原电池,负极通入
2019-11-27
甲醇(CH3OH))是一种重要的有机物,有重要的应用.
(1)甲醇作燃料燃烧的化学方程式为2CH3OH+3O2
2CO2+4H2O,该反应中化学能主要转化为___,该反应的氧化剂是___.
(2)将甲醇和氧气分别通入如图装置中形成原电池,负极通入的是___(填写化学式).溶液中的OH-移向___(填写“正”或“负”)极,若有2mol甲醇参加反应,转移电子的个数为___.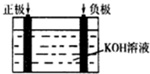
(3)已知甲醇燃料电池每生成1mol的液态水放出a kJ热量,又知该电池每发1kW•h电能生成b g水,则该电池的能量转化率为___.
(1)甲醇作燃料燃烧的化学方程式为2CH3OH+3O2
| ||
(2)将甲醇和氧气分别通入如图装置中形成原电池,负极通入的是___(填写化学式).溶液中的OH-移向___(填写“正”或“负”)极,若有2mol甲醇参加反应,转移电子的个数为___.

(3)已知甲醇燃料电池每生成1mol的液态水放出a kJ热量,又知该电池每发1kW•h电能生成b g水,则该电池的能量转化率为___.