如图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置.其中E瓶中放有干燥红色布条;F中为铜网,F右端出气管口附近放有脱脂棉.试回答:(1)A试剂为,B试剂为,化学方程式为MnO2+4HCl(浓) △ . MnCl2+Cl2↑+2H2OMnO2+4HCl(浓) △ . MnCl2+Cl2↑+2H2O;(2)C试剂为;D试剂作用为;(3)E中干燥红色布条(填“褪色”或“不褪色”);(4)F
2019-06-19
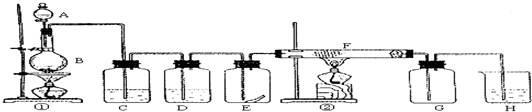
如图为实验室制取纯净、干燥的Cl2,并进行检验Cl2性质实验的装置.其中E瓶中放有干燥红色布条;F中为铜网,F右端出气管口附近放有脱脂棉.
试回答:
(1)A试剂为______,B试剂为______,化学方程式为MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
(2)C试剂为______;D试剂作用为______;
(3)E中干燥红色布条______(填“褪色”或“不褪色”);
(4)F管中现象______,脱脂棉的作用是______;
(5)H中试剂为______,化学方程式为______.
优质解答
根据题中所给出的信息可知本实验是室制取纯净、干燥的Cl2,并进行检验Cl2性质实验.
(1)实验室制备氯气用的是浓盐酸和固体MnO2的加热反应,所以A为浓盐酸,B为MnO2,反应的化学方程式为:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,
故答案为:浓盐酸;MnO2;MnO2+4HCl-MnCl2+Cl2↑+2H2O;
(2)浓盐酸具有挥发性,所以由①中生成氯气中含有挥发出的HCl气体,食盐溶于水后电离出氯离子,抑制氯气和水反应,降低氯气的溶解度,除去HCl气体用饱和食盐水,因此C为饱和食盐水;氯气从C中通入到D中进行干燥出去氯气的水蒸气,D中是浓硫酸,
故答案为:饱和食盐水;吸水氯气中的水蒸气;
(3)氯气从D中出来后是干燥的氯气,通到E中,干燥的氯气不能漂白,因此E中的干燥布条不褪色,
故答案为:不褪色;
(4)已知F中是铜网,在加热的条件下,氯气与Cu发生反应,生成棕黄色的烟.脱脂棉的作用是为了防止防止CuCl2固体小颗粒被气体鼓入导管中,堵塞导管,影响氯气的收集,
故答案为:棕黄色的烟;防止生成的氯化铜颗粒堵塞导管;
(5)氯气是有毒气体,所以H中是吸收多余气体的NaOH溶液,反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:NaOH溶液;Cl2+2NaOH=NaCl+NaClO+H2O;
根据题中所给出的信息可知本实验是室制取纯净、干燥的Cl2,并进行检验Cl2性质实验.
(1)实验室制备氯气用的是浓盐酸和固体MnO2的加热反应,所以A为浓盐酸,B为MnO2,反应的化学方程式为:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,
故答案为:浓盐酸;MnO2;MnO2+4HCl-MnCl2+Cl2↑+2H2O;
(2)浓盐酸具有挥发性,所以由①中生成氯气中含有挥发出的HCl气体,食盐溶于水后电离出氯离子,抑制氯气和水反应,降低氯气的溶解度,除去HCl气体用饱和食盐水,因此C为饱和食盐水;氯气从C中通入到D中进行干燥出去氯气的水蒸气,D中是浓硫酸,
故答案为:饱和食盐水;吸水氯气中的水蒸气;
(3)氯气从D中出来后是干燥的氯气,通到E中,干燥的氯气不能漂白,因此E中的干燥布条不褪色,
故答案为:不褪色;
(4)已知F中是铜网,在加热的条件下,氯气与Cu发生反应,生成棕黄色的烟.脱脂棉的作用是为了防止防止CuCl2固体小颗粒被气体鼓入导管中,堵塞导管,影响氯气的收集,
故答案为:棕黄色的烟;防止生成的氯化铜颗粒堵塞导管;
(5)氯气是有毒气体,所以H中是吸收多余气体的NaOH溶液,反应的化学方程式为Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:NaOH溶液;Cl2+2NaOH=NaCl+NaClO+H2O;

