元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分. 族周期ⅠA011H1.008ⅡAⅢAⅣAⅤAⅥAⅦA2He4.00323Li6.9914Be9.0125B10.816C12.017N14.018O16.009F19.0010Ne20.18311Na22.9912Mg24.3113Al26.9814Si28.0915P30.9716S32.0617Cl35.4518Ar39.95(1)请从上表中查出地壳中含量最多的金属元素的相对原子质量为.(2)表中不同种元素最本质的区别是(填序号):A.
2019-06-25
元素周期表是学习和研究化学的重要工具,如图是元素周期表的一部分.
(1)请从上表中查出地壳中含量最多的金属元素的相对原子质量为______.
(2)表中不同种元素最本质的区别是______(填序号):
A.相对原子质量不同 B.质子数不同 C.中子数不同
(3)根据表中的内容总结出一条元素周期表中各元素的排列规律______.
(4)如图是五种粒子的结构示意图
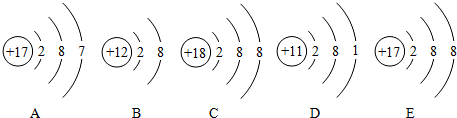
①图中粒子共能表示______种元素.A所表示的元素于______元素(填金属或非金属).
②图中表示的阳离子的是______(用序号表示).
③图中表示的阳离子和阴离子形成化合物是______(填化学式).
| 族 周期 | ⅠA | 0 | ||||||
| 1 | 1H 1.008 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 2He 4.003 |
| 2 | 3Li 6.991 | 4Be 9.012 | 5B 10.81 | 6C 12.01 | 7N 14.01 | 8O 16.00 | 9F 19.00 | 10Ne 20.18 |
| 3 | 11Na 22.99 | 12Mg 24.31 | 13Al 26.98 | 14Si 28.09 | 15P 30.97 | 16S 32.06 | 17Cl 35.45 | 18Ar 39.95 |
(2)表中不同种元素最本质的区别是______(填序号):
A.相对原子质量不同 B.质子数不同 C.中子数不同
(3)根据表中的内容总结出一条元素周期表中各元素的排列规律______.
(4)如图是五种粒子的结构示意图

①图中粒子共能表示______种元素.A所表示的元素于______元素(填金属或非金属).
②图中表示的阳离子的是______(用序号表示).
③图中表示的阳离子和阴离子形成化合物是______(填化学式).