(6分)元素周期表是学习化学的重要工具,下表是元素周期表的一部分。请回答下列问题: 1 H 2 He 3 Li 4 Be 5 B 6 C 7 N 8 O 9 F 10 Ne 11 Na 12 Mg 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar (1)元素周期表中不同种元素最本质的区别是 (填序号)。A.相对原子质量不同
2019-06-25
| (6分)元素周期表是学习化学的重要工具,下表是元素周期表的一部分。请回答下列问题:
(1)元素周期表中不同种元素最本质的区别是 (填序号)。 A.相对原子质量不同 B.质子数不同 C.中子数不同 (2)镁元素的原子结构示意图为 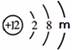 ,则m = ,该原子在化学反应中易 ,则m = ,该原子在化学反应中易(填“得到”或“失去”)电子。说明元素的化学性质与原子的 关系密切。 (3)元素周期表中每一个横行叫做一个周期。以第二周期为例,根据图-6该周期中各元素的原子结构示意图,分析同一周期元素之间的排列有一定的规律,如: (填序号)。 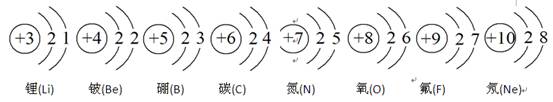 A.从左到右,各元素原子的电子层数相同 B.从左到右,各元素的原子序数依次递增 C.从左到右,各元素原子的最外层电子数相同 (4)由1号和8号元素组成的化合物(分子中原子个数比为2:1)与6号元素的单质,在高温下发生置换反应,生成一种最轻的气体和一种由双原子分子构成的化合物,该反应的化学方程式是__ __。 | ||||||||||||||||||||||||