根据下列框图回答有关问题(答题时,方程式中的E用所对应的元素符号表示): 已知:Na 2 EO 2 溶于过量的新制氯水,形成黄色溶液,向该溶液中滴加KSCN溶液立即出现红色,振荡,一段时间后,红色褪去.(1)A的电子式为.(2)写出反应②的化学方程式.(3)写出Na 2 EO 2 与新制氯水反应的离子方程式.(4)一段时间后红色褪去的原因可能是:①E元素被氯水氧化为更高价态的物质;②.
2019-11-27
根据下列框图回答有关问题(答题时,方程式中的E用所对应的元素符号表示):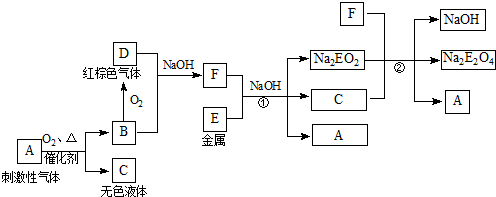 已知:Na 2 EO 2 溶于过量的新制氯水,形成黄色溶液,向该溶液中滴加KSCN溶液立即出现红色,振荡,一段时间后,红色褪去. (1)A的电子式为______. (2)写出反应②的化学方程式______. (3)写出Na 2 EO 2 与新制氯水反应的离子方程式______. (4)一段时间后红色褪去的原因可能是: ①E元素被氯水氧化为更高价态的物质;②______. |
