钛及其化合物大量应用于航空、造船、电子、化学、医疗器械、电讯器材等各个领域.由钛铁矿(FeTiO3)提取金属钛(海绵钛)的主要工艺流程如下(部分产物省略):(1)氯化的过程是将二氧化钛、碳粉混合,在高温条件下通人氯气制得TiCl4和一种可燃性气体,该反应的化学方程式为;TiCl4在室温下为无色液体,氯化后提纯四氯化钛的方法是过滤、.(2)还原过程是用过量的镁在高温条件下与TiCl4反应制得海绵钛.写出此反应的化学方程式.(3)还原过程必须在1070K的温度下进行,你认为还应该控制的反应条件是.(4)常温下
2019-04-14
钛及其化合物大量应用于航空、造船、电子、化学、医疗器械、电讯器材等各个领域.由钛铁矿(FeTiO3)提取金属钛(海绵钛)的主要工艺流程如下(部分产物省略):
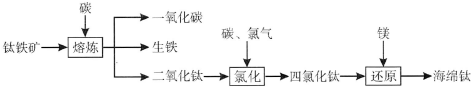
(1)氯化的过程是将二氧化钛、碳粉混合,在高温条件下通人氯气制得TiCl4和一种可燃性气体,该反应的化学方程式为___;TiCl4在室温下为无色液体,氯化后提纯四氯化钛的方法是过滤、___.
(2)还原过程是用过量的镁在高温条件下与TiCl4反应制得海绵钛.写出此反应的化学方程式___.
(3)还原过程必须在1070K的温度下进行,你认为还应该控制的反应条件是___.
(4)常温下,钛不与水、稀盐酸、稀H2SO4或稀HNO3作周,但易溶于氢氟酸,推测其原因是___.
A.氢氟酸的酸性比其他酸强 B.氢氟酸的氧化性比其他酸强
C.氢氟酸的还原性比其他酸强 D.钛离子易与氟离子形成可溶性难电离物质
(5)上述工艺中,得到的海绵钛中可能含有金属镁,常温下除去该杂质应选用的试剂是稀盐酸或稀硫酸,不选择稀硝酸的原因是___;若杂质只有金属镁的某海绵钛样品,去除杂质后质量减少十分之一,则该样品中n(Ti):n(Mg)=___.

(1)氯化的过程是将二氧化钛、碳粉混合,在高温条件下通人氯气制得TiCl4和一种可燃性气体,该反应的化学方程式为___;TiCl4在室温下为无色液体,氯化后提纯四氯化钛的方法是过滤、___.
(2)还原过程是用过量的镁在高温条件下与TiCl4反应制得海绵钛.写出此反应的化学方程式___.
(3)还原过程必须在1070K的温度下进行,你认为还应该控制的反应条件是___.
(4)常温下,钛不与水、稀盐酸、稀H2SO4或稀HNO3作周,但易溶于氢氟酸,推测其原因是___.
A.氢氟酸的酸性比其他酸强 B.氢氟酸的氧化性比其他酸强
C.氢氟酸的还原性比其他酸强 D.钛离子易与氟离子形成可溶性难电离物质
(5)上述工艺中,得到的海绵钛中可能含有金属镁,常温下除去该杂质应选用的试剂是稀盐酸或稀硫酸,不选择稀硝酸的原因是___;若杂质只有金属镁的某海绵钛样品,去除杂质后质量减少十分之一,则该样品中n(Ti):n(Mg)=___.