实验是化学的灵魂,是学好化学的重要方法.(1)实验甲的实验目的是探究碳的性;实验乙观察到纸花变红,能否得出水能与二氧化碳反应的实验结论?;实验丙观察到气球B的变化情况为.(2)《酸、碱的化学性质》实验中,向两支试管中各加入相同量的氢氧化钙粉末,然后各加入1mL水,振荡,再滴入1~2滴酚酞试液.继续向其中一支试管中加入1mL盐酸,向另一支中继续加1mL水,观察现象.以上实验得出氢氧化钙的化学性质有,继续加1mL水的目的是;要得出氢氧化钙微溶于水的实验结论,实验中取用氢氧化钙时要做到.
2019-04-20
实验是化学的灵魂,是学好化学的重要方法.
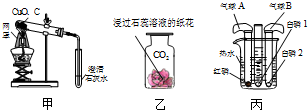
(1)实验甲的实验目的是探究碳的______性;实验乙观察到纸花变红,能否得出水能与二氧化碳反应的实验结论?______;实验丙观察到气球B的变化情况为______.
(2)《酸、碱的化学性质》实验中,向两支试管中各加入相同量的氢氧化钙粉末,然后各加入1mL水,振荡,再滴入1~2滴酚酞试液.继续向其中一支试管中加入1mL盐酸,向另一支中继续加1mL水,观察现象.以上实验得出氢氧化钙的化学性质有______,继续加1mL水的目的是______;要得出氢氧化钙微溶于水的实验结论,实验中取用氢氧化钙时要做到______.

(1)实验甲的实验目的是探究碳的______性;实验乙观察到纸花变红,能否得出水能与二氧化碳反应的实验结论?______;实验丙观察到气球B的变化情况为______.
(2)《酸、碱的化学性质》实验中,向两支试管中各加入相同量的氢氧化钙粉末,然后各加入1mL水,振荡,再滴入1~2滴酚酞试液.继续向其中一支试管中加入1mL盐酸,向另一支中继续加1mL水,观察现象.以上实验得出氢氧化钙的化学性质有______,继续加1mL水的目的是______;要得出氢氧化钙微溶于水的实验结论,实验中取用氢氧化钙时要做到______.