GB/T 4789.6-2003
基本信息
标准号: GB/T 4789.6-2003
中文名称:食品卫生微生物学检验 致泻大肠埃希氏菌检验
标准类别:国家标准(GB)
英文名称:Microbiological examination of food hygiene-Examination of diarrheogenic Escherichia coli
标准状态:已作废
发布日期:2003-08-01
实施日期:2004-01-01
作废日期:2017-06-23
下载格式:pdf zip

标准分类号
标准ICS号: 数学、自然科学>>微生物学>>07.100.30
中标分类号:医药、卫生、劳动保护>>卫生>>C53食品卫生
关联标准
出版信息
出版社:中国标准出版社
页数:8页
标准价格:29.0
出版日期:2004-01-01
相关单位信息
首发日期:1984-12-25
复审日期:2004-10-14
起草人:何晓青、冉陆、付萍、姚景会
起草单位:江西省卫防站、中国疾病预防控制中心营养与食品安全所
归口单位:中华人民共和国卫生部
提出单位:中华人民共和国卫生部
发布部门:中华人民共和国卫生部、中国国家标准化管理委员会
主管部门:卫生部
标准简介
本标准规定了食品中致泻大肠埃希氏菌的检验方法。本标准适用于食品和食物中毒样品中致泻大肠埃希氏菌的检验。
标准图片预览




标准内容
ICS07.100.30
中华人民共和国国家标准
GB/T4789.6—2003
代替GB/T4789.6—1994
食品卫生微生物学检验
致泻大肠埃希氏菌检验
Microbiological examination of food hygiene-Examination of diarrheogenic Escherichia coli2003-08-11发布
中华人民共和国卫生部
中国国家标准化管理委员会
2004-01-01实施
GB/T4789.6—2003
本标准对GB/T4789.6--1994&食品卫生微生物学检验本标准与GB/T4789.6—1994相比主要修改如下:致泻大肠埃希氏菌检验》进行修订。按照GB/T1.1一2000对标准文本的格式和文字进行修改。-修改并规范原标准中的“设备和材料”。本标准自实施之日起,GB/T4789.6—1994同时废止。本标准由中华人民共和国卫生部提出并归口。本标准起草单位:江西省卫生防疫站、中国疾病预防控制中心营养与食品安全所。本标准主要起草人:何晓青、冉陆、付葬、姚景会。本标准于1984年首次发布,1994年第一次修订,本次为第二次修订。40
1范围
食品卫生微生物学检验
致泻大肠埃希氏菌检验
本标准规定了食品中致泻大肠埃希氏菌的检验方法。本标准适用于食品和食物中毒样品中致泻大肠埃希氏菌的检验。2规范性引用文件
GB/T4789.6—2003
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T4789.28—2003食品卫生微生物学检验染色法、培养基和试剂3设备和材料
冰箱:0℃~4℃。
3.2恒温培养箱:36℃±1℃,42℃。3.3恒温水浴锅:100℃,65℃~68℃,50℃。3.4显微镜:10X~100×。
离心机:3000r/min。
3.6酶标仪。
均质器或灭菌乳钵。
架盘药物天平:0g~500g,精确至0.5g。3.94
细菌浓度比浊管:MacFarland3号。3.10灭菌广口瓶:500mL。
3.11灭菌锥形瓶:500mL,250mL。3.12灭菌吸管:1mL(具0.01mL刻度)、5mL(具0.1mL刻度)。3.13灭菌培养Ⅲ:直径90mm。
3.14灭菌试管:10mm×75mm.16mm×160mm。3.15注射器:0.25mL,连接内径为1mm塑料小管一段。3.16灭菌的刀子、剪子、镊子等。3.17小白鼠:1日~4日龄。
3.18硝酸纤维素滤膜150mm×50mm,o.45μm。临用时切成两张,每张75mm×50mm,用铅笔划格,每格6mm×6mm,每行10格,分6行。灭菌备用。41
GB/T4789.6—2003
4培养基和试剂
乳糖胆盐发酵管:按GB/T4789.28—2003中4.9规定。4.1
4.2营养肉汤:按GB/T4789.28—2003中4.8规定。4.3肠道菌增菌肉汤:按GB/T4789.28--2003中4.18规定。麦康凯琼脂:按GB/T4789.28—2003中4.24规定。4.4
伊红美蓝琼脂(EMB):按GB/T4789.28—2003中4.25规定。4.5
4.6三糖铁琼脂(TSI):按GB/T4789.28--2003中4.26,4.27规定。4.7克氏双糖铁琼脂(KI):按GB/T4789.28—2003中4.28,4.29规定。糖发酵管(乳糖、鼠李糖、木糖和甘露醇):按GB/T4789.28—2003中3.2规定。4.8
赖氮酸脱羧酶试验培养基:按GB/T4789.282003中3.12规定。4.9
4.10尿素琼脂(pH7.2):按GB/T4789.28-—2003中3.15规定。4.11氰化钾(KCN)培养基:按GB/T4789.28—2003中3.16规定。蛋白陈水、靛基质试剂:按GB/T4789.28—2003中3.13规定。4.12
半固体琼脂:按GB/T4789.28—2003中4.30规定。4.13
4.14Honda氏产毒肉汤:按GB/T4789.28—2003中4.34规定。4.15Elek氏培养基:按GB/T4789.28—2003中4.35规定。4.16氧化酶试剂:按GB/T4789.28—2003中3.18规定。4.17革兰氏染色液:按GB/T4789.28—2003中2.2规定。3致病性大肠埃希氏菌诊断血清、侵袭性大肠埃希氏菌诊断血清、产肠毒素大肠埃希氏菌诊断血4.18
清、出血性大肠埃希氏菌诊断血清。4.19产肠毒素大肠埃希氏菌LT和ST酶标诊断试剂盒。4.20产肠毒素LT和ST大肠埃希氏菌标准菌株。4.21抗LT抗毒素。
多粘菌素B纸片:300U,16mm。
4.230.1%硫柳汞溶液。
4.242%伊文思蓝溶液。
5检验程序
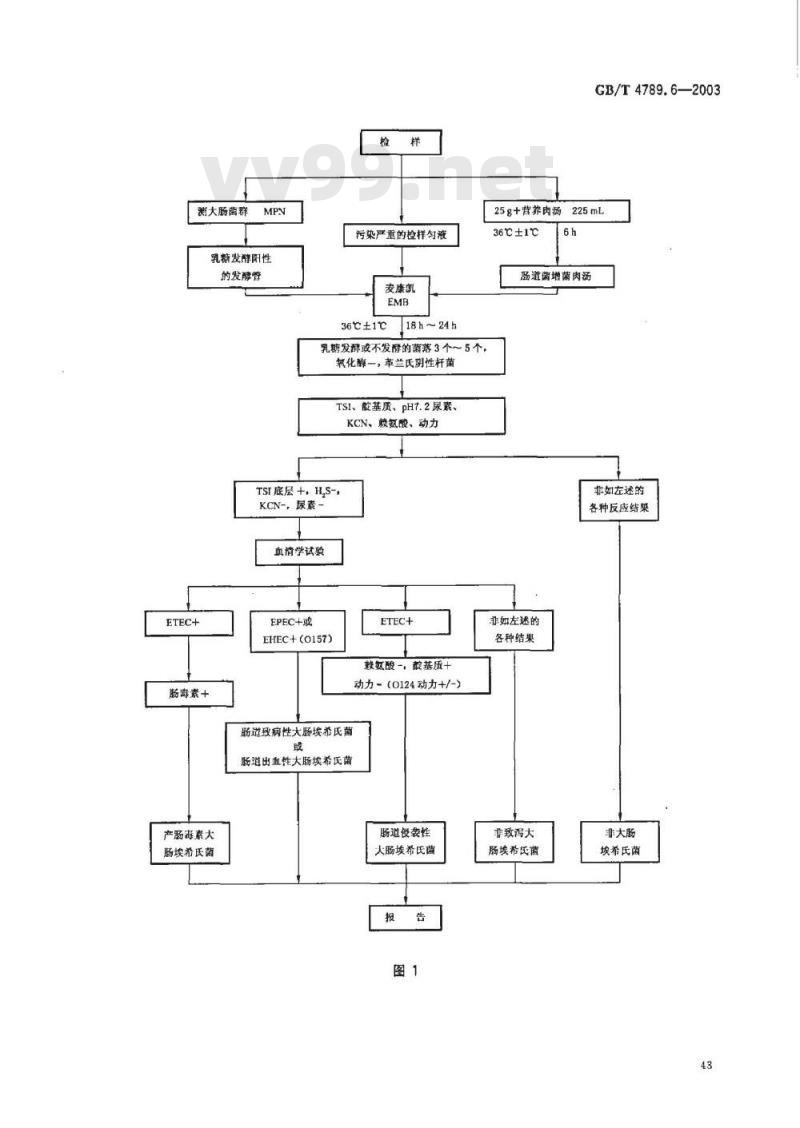
致泻大肠埃希氏菌检验程序见图1。42
谢大肠菌群MPV
乳精发醇阳性
的发酵管
污染严重的检样勾液
凌康凯
18h~24h
36±1r
GB/T4789.6—2003
25g+营养肉汤225mL
肠道菌增菌肉汤
乳糖发酵或不发酵的菌落3个~5个,氧化醇一,革兰氏阴性杆菌
TSI、靛基质、pH7.2尿素、
KCN、敲氨酸、动力
TSI底层+,HS-
KCN-,尿素-
血清学试验
肠毒素+
产肠毒素大
肠埃希氏菌
EPEC+或
EHEC+(O157)
较氨酸-,靛基质十
动力-(0124动力+/-)
肠道致病性大肠埃希氏菌
肠道出血性大肠埃希氏菌
肠道侵装性
大肠埃希氏菌
非如左述的
各种结巢
非致泻大
肠埃希氏菌
非如左述的
各种反应结
非大肠
埃希氏菌
GB/T4789.6-—2003
6操作步骤
6.1增菌
样品采集后应尽快检验。除了易腐食品在检验之前预冷藏外,一般不冷藏。以无菌操作取检样25g(mL),加在225mL营养肉汤中,以均质器打碎1min或用乳钵加灭菌砂磨碎。取出适量,接种乳糖胆盐培养基,以测定大肠菌群MPN,其余的移人500mL广口瓶内,于36℃土1℃培养6h。挑取1环,接种于1管30mL肠道菌增菌肉汤内,于42℃培养18h。6.2分离
将乳糖发酵阳性的乳糖胆盐发酵管和增菌液分别划线接种麦康凯或伊红美蓝琼脂平板:污染严重的检样,可将检样勾液直接划线接种麦康凯或伊红美蓝平板,于36℃士1℃培养18h~24h,观察菌落。不但要注意乳糖发酵的菌落,同时也要注意乳糖不发酵和迟缓发酵的菌落。6.3生化试验
6.3.1自鉴别平板上直接挑取数个菌落分别接种三糖铁琼脂(TSI)或克氏双糖铁琼脂(KI)。同时将这些塔养物分别接种蛋白藤水,半固体、PH7.2尿素琼脂,KCN肉汤和赖氨酸脱羧酶试验培养基。以上培养物均在36℃培养过夜。
6.3.2TSI斜面产酸或不产酸,底层产酸,H,S阴性,KCN阴性和尿素阴性的培养物为大肠埃希氏菌。TSI底层不产酸,或H2S、KCN、尿素有任一项为阳性的培养物,均非大肠埃希氏菌。必要时做氧化酶试验和革兰氏染色。vv99.net
6.4血清学试验
6.4.1假定试验:挑取经生化试验证实为大肠埃希氏菌琼脂培养物,用致病性大肠埃希氏菌、侵袭性大肠埃希氏菌和产肠毒素大肠埃希氏菌多价0血清和出血性大肠埃希氏菌O157血清做玻片凝集试验。当与某一种多价○血清凝集时,再与该多价血清所包含的单价O血清做试验。致泻大肠埃希氏菌所包括的O抗原群见表1。如与某一个单价○血清呈现强凝集反应,即为假定试验阳性。表1致泻大肠埃希氏菌所包括的0抗原群大肠埃希氏菌的种类
所包括的0抗原群
026055086011lab011401190125ac01270128ab01420158
028ac029
0112ac0115012401350136014301440167
06011015
06307808501140115
0128ac014801490159
0166Q167
6.4.2证实试验:制备0抗原悬液,稀释至与MacFarland3号比浊管相当的浓度。原效价为(1:160)~1:320)的0血清,用0.5%盐水稀释至1:40。稀释血清与抗原悬液在10mm×75mm试管内等量混合,做单管凝集试验。混匀后放于50℃水浴锅内,经16h后观察结果。如出现凝集,可证实为该○抗原。
6.5肠毒索试验
6.5.1酶联免疫吸附试验检测LT和ST6.5.1.1产毒培养:将试验菌株和阳性及阴性对照菌株分别接种于0.6mLCAYE培养基内,37℃振荡培养过夜。加人20000IU/mL的多粘菌素B0.05mL,于37℃1h,离心4000r/min15min,分离上清液,加人0.1%硫柳汞0.05mL,于4℃保存待用。6.5.1.2LT检测方法(双抗体夹心法):包被:先在产肠毒素大肠埃希氏菌LT和ST酶标诊断试剂盒中取出包被用LT抗体管,加人a)
GB/T4789.6—2003
包被液0.5mL,混勾后全部吸出于3.6mL包被液中混匀,以每孔100μL量加人到40孔聚苯乙烯硬反应板中,第一孔留空作对照,于4℃冰箱湿盒中过夜洗板:将板中溶液甩去,用洗涤液I洗三次,甩尽液体,翻转反应板,在吸水纸上拍打,去尽孔中b)
残留液体。
封闭:每孔加100μL封闭液,于37℃水浴中1h。c)
洗板:用洗涤液IⅡ洗三次,操作同上。d)
e)·加样本:每孔分别加各种试验菌株产毒培养液100μL,37℃水浴中1h。洗板:用洗涤液Ⅱ洗三次,操作同上。f)
加酶标抗体:先在酶标LT抗体管中加0.5mL稀释液,混勾后全部吸出于3.6mL稀释液中g)
混匀,每孔加100μL,37℃水浴中1h。洗板:用洗涤液Ⅱ洗三次,操作同上。h)
酶底物反应:每孔(包括第一孔)各加基质液100μL,室温下避光作用5min10min,加入终止i)
液50L。
j)结果判定:以酶标仪在波长492nm下测定吸光度OD值,待测标本OD值大于阴性对照3倍以上为阳性,目测颜色为桔黄色或明显高于阴性对照为阳性。6.5.1.3ST检测方法(抗原竞争法):包被:先在包被用ST抗原管中加0.5mL包被液,混匀后全部吸出于1.6mL包被液中混匀,a
以每孔50μL加人于40孔聚苯乙烯软反应板中。加液后轻轻敲板,使液体布满孔底。第一孔留空作对照,置4℃冰箱湿盒中过夜。洗板:用洗涤液I洗三次,操作同上。b)
封闭:每孔加100μL封闭液,37℃水浴1h。e
洗板:用洗涤液Ⅱ洗三次,操作同上。d)
加样本及ST单克隆抗体:每孔分别加各试验菌株产毒培养液50μL,稀释的ST单克隆抗体e)
50μL(先在ST单克隆抗体管中加0.5mL稀释液,混匀后全部吸出于1.6mL稀释液中,混匀备用),37℃水浴1h。
f)洗板:用洗涤液Ⅱ洗三次,操作同上。加酶标记兔抗鼠Ig复合物:先在酶标记免抗鼠Ig复合物管中加0.5mL稀释液,混匀后全部吸g)
出于3.6mL稀释液中混匀,每孔加100μL,37℃水浴1h。洗板用洗涤液ⅡI洗三次,操作同上。h)
酶底物反应,每孔(包括第一孔)各加基质液100μL,室温下避光5min~10min,再加入终止液50μL。
j)结果判定:以酶标仪在波长492nm下测定吸光度(OD)值,计算见式(1):吸光度=阴性对照性停量货测样本OD值×100%阴性对照OD值
吸光度大于等于50%为阳性。目测无色或明显淡于阴性对照为阳性。6.5.2双向琼脂扩散试验检测L1
...(1)
将被检菌株按五点环形接种于Elek氏培养基上。以同样操作,共做两份,于36℃培养48h。在每株菌的菌苔上放多粘菌素B纸片,于36℃经5h~6h,使肠毒素渗人琼脂中,在五点环形菌苔各5mm处的中央,挖一个直径4mm的圆孔,并用一滴琼脂垫底。在平板的中央孔内滴加LT抗毒素30μL,用已知产LT和不产毒菌株作对照,于36℃经15h~20h观察结果。在菌斑和抗毒素孔之间出现白色沉淀带者为阳性,无沉淀带者为阴性。6.5.3乳鼠灌胃试验检测ST
将被检菌株接种于Honda氏产毒肉汤内,于36℃培养24h,以3000r/min离心30min,取上清液45
GB/T4789.6—2003
经薄膜滤器过滤,加热60℃30min,每1mL滤液内加人2%伊文思蓝溶液0.02mL。将此滤液用塑料小管注人1日~4日龄的乳鼠胃内0.1mL,同时接种3只~4只,禁食3h~4h后用三氯甲烷麻醉,取出全部肠管,称量肠管(包括积液)重量及剩余体重。肠管重量与剩余体重之比大于0.09为阳性,0.07~0.09为可疑。
6.6结果报告
综合以上生化试验、血清学试验、肠毒素试验作出报告。46
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民共和国国家标准
GB/T4789.6—2003
代替GB/T4789.6—1994
食品卫生微生物学检验
致泻大肠埃希氏菌检验
Microbiological examination of food hygiene-Examination of diarrheogenic Escherichia coli2003-08-11发布
中华人民共和国卫生部
中国国家标准化管理委员会
2004-01-01实施
GB/T4789.6—2003
本标准对GB/T4789.6--1994&食品卫生微生物学检验本标准与GB/T4789.6—1994相比主要修改如下:致泻大肠埃希氏菌检验》进行修订。按照GB/T1.1一2000对标准文本的格式和文字进行修改。-修改并规范原标准中的“设备和材料”。本标准自实施之日起,GB/T4789.6—1994同时废止。本标准由中华人民共和国卫生部提出并归口。本标准起草单位:江西省卫生防疫站、中国疾病预防控制中心营养与食品安全所。本标准主要起草人:何晓青、冉陆、付葬、姚景会。本标准于1984年首次发布,1994年第一次修订,本次为第二次修订。40
1范围
食品卫生微生物学检验
致泻大肠埃希氏菌检验
本标准规定了食品中致泻大肠埃希氏菌的检验方法。本标准适用于食品和食物中毒样品中致泻大肠埃希氏菌的检验。2规范性引用文件
GB/T4789.6—2003
下列文件中的条款通过本标准的引用而成为本标准的条款。凡是注日期的引用文件,其随后所有的修改单(不包括勘误的内容)或修订版均不适用于本标准,然而,鼓励根据本标准达成协议的各方研究是否可使用这些文件的最新版本。凡是不注日期的引用文件,其最新版本适用于本标准。GB/T4789.28—2003食品卫生微生物学检验染色法、培养基和试剂3设备和材料
冰箱:0℃~4℃。
3.2恒温培养箱:36℃±1℃,42℃。3.3恒温水浴锅:100℃,65℃~68℃,50℃。3.4显微镜:10X~100×。
离心机:3000r/min。
3.6酶标仪。
均质器或灭菌乳钵。
架盘药物天平:0g~500g,精确至0.5g。3.94
细菌浓度比浊管:MacFarland3号。3.10灭菌广口瓶:500mL。
3.11灭菌锥形瓶:500mL,250mL。3.12灭菌吸管:1mL(具0.01mL刻度)、5mL(具0.1mL刻度)。3.13灭菌培养Ⅲ:直径90mm。
3.14灭菌试管:10mm×75mm.16mm×160mm。3.15注射器:0.25mL,连接内径为1mm塑料小管一段。3.16灭菌的刀子、剪子、镊子等。3.17小白鼠:1日~4日龄。
3.18硝酸纤维素滤膜150mm×50mm,o.45μm。临用时切成两张,每张75mm×50mm,用铅笔划格,每格6mm×6mm,每行10格,分6行。灭菌备用。41
GB/T4789.6—2003
4培养基和试剂
乳糖胆盐发酵管:按GB/T4789.28—2003中4.9规定。4.1
4.2营养肉汤:按GB/T4789.28—2003中4.8规定。4.3肠道菌增菌肉汤:按GB/T4789.28--2003中4.18规定。麦康凯琼脂:按GB/T4789.28—2003中4.24规定。4.4
伊红美蓝琼脂(EMB):按GB/T4789.28—2003中4.25规定。4.5
4.6三糖铁琼脂(TSI):按GB/T4789.28--2003中4.26,4.27规定。4.7克氏双糖铁琼脂(KI):按GB/T4789.28—2003中4.28,4.29规定。糖发酵管(乳糖、鼠李糖、木糖和甘露醇):按GB/T4789.28—2003中3.2规定。4.8
赖氮酸脱羧酶试验培养基:按GB/T4789.282003中3.12规定。4.9
4.10尿素琼脂(pH7.2):按GB/T4789.28-—2003中3.15规定。4.11氰化钾(KCN)培养基:按GB/T4789.28—2003中3.16规定。蛋白陈水、靛基质试剂:按GB/T4789.28—2003中3.13规定。4.12
半固体琼脂:按GB/T4789.28—2003中4.30规定。4.13
4.14Honda氏产毒肉汤:按GB/T4789.28—2003中4.34规定。4.15Elek氏培养基:按GB/T4789.28—2003中4.35规定。4.16氧化酶试剂:按GB/T4789.28—2003中3.18规定。4.17革兰氏染色液:按GB/T4789.28—2003中2.2规定。3致病性大肠埃希氏菌诊断血清、侵袭性大肠埃希氏菌诊断血清、产肠毒素大肠埃希氏菌诊断血4.18
清、出血性大肠埃希氏菌诊断血清。4.19产肠毒素大肠埃希氏菌LT和ST酶标诊断试剂盒。4.20产肠毒素LT和ST大肠埃希氏菌标准菌株。4.21抗LT抗毒素。
多粘菌素B纸片:300U,16mm。
4.230.1%硫柳汞溶液。
4.242%伊文思蓝溶液。
5检验程序
致泻大肠埃希氏菌检验程序见图1。42
谢大肠菌群MPV
乳精发醇阳性
的发酵管
污染严重的检样勾液
凌康凯
18h~24h
36±1r
GB/T4789.6—2003
25g+营养肉汤225mL
肠道菌增菌肉汤
乳糖发酵或不发酵的菌落3个~5个,氧化醇一,革兰氏阴性杆菌
TSI、靛基质、pH7.2尿素、
KCN、敲氨酸、动力
TSI底层+,HS-
KCN-,尿素-
血清学试验
肠毒素+
产肠毒素大
肠埃希氏菌
EPEC+或
EHEC+(O157)
较氨酸-,靛基质十
动力-(0124动力+/-)
肠道致病性大肠埃希氏菌
肠道出血性大肠埃希氏菌
肠道侵装性
大肠埃希氏菌
非如左述的
各种结巢
非致泻大
肠埃希氏菌
非如左述的
各种反应结
非大肠
埃希氏菌
GB/T4789.6-—2003
6操作步骤
6.1增菌
样品采集后应尽快检验。除了易腐食品在检验之前预冷藏外,一般不冷藏。以无菌操作取检样25g(mL),加在225mL营养肉汤中,以均质器打碎1min或用乳钵加灭菌砂磨碎。取出适量,接种乳糖胆盐培养基,以测定大肠菌群MPN,其余的移人500mL广口瓶内,于36℃土1℃培养6h。挑取1环,接种于1管30mL肠道菌增菌肉汤内,于42℃培养18h。6.2分离
将乳糖发酵阳性的乳糖胆盐发酵管和增菌液分别划线接种麦康凯或伊红美蓝琼脂平板:污染严重的检样,可将检样勾液直接划线接种麦康凯或伊红美蓝平板,于36℃士1℃培养18h~24h,观察菌落。不但要注意乳糖发酵的菌落,同时也要注意乳糖不发酵和迟缓发酵的菌落。6.3生化试验
6.3.1自鉴别平板上直接挑取数个菌落分别接种三糖铁琼脂(TSI)或克氏双糖铁琼脂(KI)。同时将这些塔养物分别接种蛋白藤水,半固体、PH7.2尿素琼脂,KCN肉汤和赖氨酸脱羧酶试验培养基。以上培养物均在36℃培养过夜。
6.3.2TSI斜面产酸或不产酸,底层产酸,H,S阴性,KCN阴性和尿素阴性的培养物为大肠埃希氏菌。TSI底层不产酸,或H2S、KCN、尿素有任一项为阳性的培养物,均非大肠埃希氏菌。必要时做氧化酶试验和革兰氏染色。vv99.net
6.4血清学试验
6.4.1假定试验:挑取经生化试验证实为大肠埃希氏菌琼脂培养物,用致病性大肠埃希氏菌、侵袭性大肠埃希氏菌和产肠毒素大肠埃希氏菌多价0血清和出血性大肠埃希氏菌O157血清做玻片凝集试验。当与某一种多价○血清凝集时,再与该多价血清所包含的单价O血清做试验。致泻大肠埃希氏菌所包括的O抗原群见表1。如与某一个单价○血清呈现强凝集反应,即为假定试验阳性。表1致泻大肠埃希氏菌所包括的0抗原群大肠埃希氏菌的种类
所包括的0抗原群
026055086011lab011401190125ac01270128ab01420158
028ac029
0112ac0115012401350136014301440167
06011015
06307808501140115
0128ac014801490159
0166Q167
6.4.2证实试验:制备0抗原悬液,稀释至与MacFarland3号比浊管相当的浓度。原效价为(1:160)~1:320)的0血清,用0.5%盐水稀释至1:40。稀释血清与抗原悬液在10mm×75mm试管内等量混合,做单管凝集试验。混匀后放于50℃水浴锅内,经16h后观察结果。如出现凝集,可证实为该○抗原。
6.5肠毒索试验
6.5.1酶联免疫吸附试验检测LT和ST6.5.1.1产毒培养:将试验菌株和阳性及阴性对照菌株分别接种于0.6mLCAYE培养基内,37℃振荡培养过夜。加人20000IU/mL的多粘菌素B0.05mL,于37℃1h,离心4000r/min15min,分离上清液,加人0.1%硫柳汞0.05mL,于4℃保存待用。6.5.1.2LT检测方法(双抗体夹心法):包被:先在产肠毒素大肠埃希氏菌LT和ST酶标诊断试剂盒中取出包被用LT抗体管,加人a)
GB/T4789.6—2003
包被液0.5mL,混勾后全部吸出于3.6mL包被液中混匀,以每孔100μL量加人到40孔聚苯乙烯硬反应板中,第一孔留空作对照,于4℃冰箱湿盒中过夜洗板:将板中溶液甩去,用洗涤液I洗三次,甩尽液体,翻转反应板,在吸水纸上拍打,去尽孔中b)
残留液体。
封闭:每孔加100μL封闭液,于37℃水浴中1h。c)
洗板:用洗涤液IⅡ洗三次,操作同上。d)
e)·加样本:每孔分别加各种试验菌株产毒培养液100μL,37℃水浴中1h。洗板:用洗涤液Ⅱ洗三次,操作同上。f)
加酶标抗体:先在酶标LT抗体管中加0.5mL稀释液,混勾后全部吸出于3.6mL稀释液中g)
混匀,每孔加100μL,37℃水浴中1h。洗板:用洗涤液Ⅱ洗三次,操作同上。h)
酶底物反应:每孔(包括第一孔)各加基质液100μL,室温下避光作用5min10min,加入终止i)
液50L。
j)结果判定:以酶标仪在波长492nm下测定吸光度OD值,待测标本OD值大于阴性对照3倍以上为阳性,目测颜色为桔黄色或明显高于阴性对照为阳性。6.5.1.3ST检测方法(抗原竞争法):包被:先在包被用ST抗原管中加0.5mL包被液,混匀后全部吸出于1.6mL包被液中混匀,a
以每孔50μL加人于40孔聚苯乙烯软反应板中。加液后轻轻敲板,使液体布满孔底。第一孔留空作对照,置4℃冰箱湿盒中过夜。洗板:用洗涤液I洗三次,操作同上。b)
封闭:每孔加100μL封闭液,37℃水浴1h。e
洗板:用洗涤液Ⅱ洗三次,操作同上。d)
加样本及ST单克隆抗体:每孔分别加各试验菌株产毒培养液50μL,稀释的ST单克隆抗体e)
50μL(先在ST单克隆抗体管中加0.5mL稀释液,混匀后全部吸出于1.6mL稀释液中,混匀备用),37℃水浴1h。
f)洗板:用洗涤液Ⅱ洗三次,操作同上。加酶标记兔抗鼠Ig复合物:先在酶标记免抗鼠Ig复合物管中加0.5mL稀释液,混匀后全部吸g)
出于3.6mL稀释液中混匀,每孔加100μL,37℃水浴1h。洗板用洗涤液ⅡI洗三次,操作同上。h)
酶底物反应,每孔(包括第一孔)各加基质液100μL,室温下避光5min~10min,再加入终止液50μL。
j)结果判定:以酶标仪在波长492nm下测定吸光度(OD)值,计算见式(1):吸光度=阴性对照性停量货测样本OD值×100%阴性对照OD值
吸光度大于等于50%为阳性。目测无色或明显淡于阴性对照为阳性。6.5.2双向琼脂扩散试验检测L1
...(1)
将被检菌株按五点环形接种于Elek氏培养基上。以同样操作,共做两份,于36℃培养48h。在每株菌的菌苔上放多粘菌素B纸片,于36℃经5h~6h,使肠毒素渗人琼脂中,在五点环形菌苔各5mm处的中央,挖一个直径4mm的圆孔,并用一滴琼脂垫底。在平板的中央孔内滴加LT抗毒素30μL,用已知产LT和不产毒菌株作对照,于36℃经15h~20h观察结果。在菌斑和抗毒素孔之间出现白色沉淀带者为阳性,无沉淀带者为阴性。6.5.3乳鼠灌胃试验检测ST
将被检菌株接种于Honda氏产毒肉汤内,于36℃培养24h,以3000r/min离心30min,取上清液45
GB/T4789.6—2003
经薄膜滤器过滤,加热60℃30min,每1mL滤液内加人2%伊文思蓝溶液0.02mL。将此滤液用塑料小管注人1日~4日龄的乳鼠胃内0.1mL,同时接种3只~4只,禁食3h~4h后用三氯甲烷麻醉,取出全部肠管,称量肠管(包括积液)重量及剩余体重。肠管重量与剩余体重之比大于0.09为阳性,0.07~0.09为可疑。
6.6结果报告
综合以上生化试验、血清学试验、肠毒素试验作出报告。46
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。