甲醇是一种可再生能源,具有开发和应用的广阔前景,2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池方面取得了新的突破.甲醇燃料电池的工作原理如图甲装置所示.(1)甲醇进入极(填“正”或“负”).(2)工作一段时间后,当0.2mol甲醇完全反应生成CO2时,有NA的电子转移.(3)若甲装置中“负载”为右图乙装置,则:A(Pt)电极的反应式为,乙装置中总反应化学方程式为.若乙装置溶液体积为500mL,且忽略电解过程中溶液体积的变化,A极的质量增加5.40g时,乙装置中所得溶液的H+的浓度为:.
2019-11-27
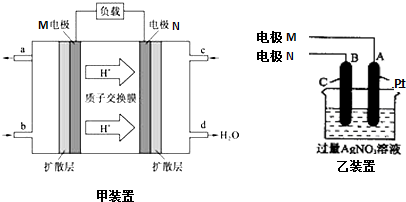
甲醇是一种可再生能源,具有开发和应用的广阔前景,2009年10月,中国科学院长春应用化学研究所在甲醇燃料电池方面取得了新的突破.甲醇燃料电池的工作原理如图甲装置所示.
(1)甲醇进入___极(填“正”或“负”).
(2)工作一段时间后,当0.2mol甲醇完全反应生成CO2时,有___NA的电子转移.
(3)若甲装置中“负载”为右图乙装置,则:A(Pt)电极的反应式为___,
乙装置中总反应化学方程式为___.若乙装置溶液体积为500mL,且忽略电解过程中溶液体积的变化,A极的质量增加5.40g时,乙装置中所得溶液的H+的浓度为:___.
(1)甲醇进入___极(填“正”或“负”).
(2)工作一段时间后,当0.2mol甲醇完全反应生成CO2时,有___NA的电子转移.
(3)若甲装置中“负载”为右图乙装置,则:A(Pt)电极的反应式为___,
乙装置中总反应化学方程式为___.若乙装置溶液体积为500mL,且忽略电解过程中溶液体积的变化,A极的质量增加5.40g时,乙装置中所得溶液的H+的浓度为:___.
