将0.1mol MnO2粉末加入到50mL过氧化氢溶液(H2O2,ρ=1.1g/mL)中,在标准状况下放出气体的体积和时间的关系如图所示. (1)实验时放出气体的总体积是.(2)放出一半气体所需的时间为.(3)反应放出 3 4 体积气体所需的时间约为.(4)A,B,C,D各点反应速率的快慢顺序为(5)解释反应速率变化的原因:(6)计算H2O2初始状态的浓度.
2019-11-26
将0.1mol MnO2粉末加入到50mL过氧化氢溶液(H2O2,ρ=1.1g/mL)中,在标准状况下放出气体的体积和时间的关系如图所示.
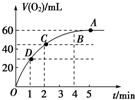
(1)实验时放出气体的总体积是___.
(2)放出一半气体所需的时间为___.
(3)反应放出
体积气体所需的时间约为___.
(4)A,B,C,D各点反应速率的快慢顺序为___
(5)解释反应速率变化的原因:___
(6)计算H2O2初始状态的浓度___.

(1)实验时放出气体的总体积是___.
(2)放出一半气体所需的时间为___.
(3)反应放出
| 3 |
| 4 |
(4)A,B,C,D各点反应速率的快慢顺序为___
(5)解释反应速率变化的原因:___
(6)计算H2O2初始状态的浓度___.