现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图.(1)a点对应的沉淀为(填化学式).(2)计算原混合液中FeCl3的物质的量浓度为多少?(写出计算过程)(3)若取原混合溶液50mL,并加入0.5mol盐酸组成新的混合溶液.往新的混合溶液中逐滴加入NaOH溶液,请在坐标内画出生成沉淀的物质的量随加入的NaOH的物质的量的关系图.
2019-04-20
现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图.
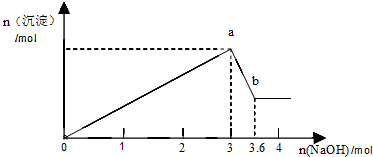
(1)a点对应的沉淀为______(填化学式).
(2)计算原混合液中FeCl3的物质的量浓度为多少?(写出计算过程)______
(3)若取原混合溶液50mL,并加入0.5mol盐酸组成新的混合溶液.往新的混合溶液中逐滴加入NaOH溶液,请在坐标内画出生成沉淀的物质的量随加入的NaOH的物质的量的关系图.
优质解答
向FeCl3、AlCl3的混合溶液中逐滴加入NaOH溶液分别发生如下反应:
AlCl3+3NaOH═Al(OH)3↓+3NaCl,FeCl3+3NaOH═Fe(OH)3↓+3NaCl,
Al(OH)3+NaOH═NaAlO2+2H2O根据反应方程式的关系得出先生成氢氧化铝、和氢氧化铁两种沉淀,体现在图象上为a点时,加入的氢氧化钠与溶液中的FeCl3、AlCl3刚好完全反应,即a点沉淀为Fe(OH)3、Al(OH)3,
故答案为:Fe(OH)3、Al(OH)3;
(2)根据图象的关系,结合反应方程式AlCl3+3NaOH═Al(OH)3↓+3NaCl,FeCl3+3NaOH═Fe(OH)3↓+3NaCl,向溶液加入3mol氢氧化钠时将,溶液中的FeCl3、AlCl3和NaOH刚好完全反应,生成Al(OH)3、Fe(OH)3沉淀,再加氢氧化钠3.6mol时,沉淀的量保持不变,又发生
Al(OH)3+NaOH═NaAlO2+2H2O,到达b点时沉淀全部为Fe(OH)3,则有:
设a点时Al(OH)3的物质的量为x mol,
Al(OH)3+NaOH═NaAlO2+2H2O
1 1
x mol (3.6-3)mol
则有:1:1=x mol:(3.6-3)mol
解得:x=0.6(mol),
设与原混合溶液中AlCl3反应的NaOH的物质的量为y mol,
AlCl3+3NaOH═Al(OH)3↓+3NaCl
3 1
y mol 0.6mol
则有:3:1=y mol:0.6 mol
解得:y=1.8(mol),
设原混合溶液中FeCl3的物质的量为z mol,
FeCl3+3NaOH═Fe(OH)3↓+3NaCl
1 3
z mol (3-1.8)mol
则有:1:3=z mol:(3-1.8)mol,
解得:z=0.4(mol),
故原混合液中FeCl3的物质的量浓度为0.4mol/0.1L=4mol/L,
故答案为:4mol/L;
(3)根据取原溶液50mL,加入0.5mol盐酸得到新溶液,其中的成分有:FeCl3、AlCl3、HCl,向其中加入NaOH溶液时,先发生HCl+NaOH═NaCl+H2O反应,当将HCl反应完后,在发生与FeCl3、AlCl3的生成沉淀,方程式为:AlCl3+3NaOH═Al(OH)3↓+3NaCl,FeCl3+3NaOH═Fe(OH)3↓+3NaCl,
完全反应后又发生反应 Al(OH)3+NaOH═NaAlO2+2H2O.
设50mL原溶液中FeCl3、AlCl3的物质的量分别为:0.2mol、0.3mol,
设中和0.5molHCl消耗的NaOH物质的量为xmol,则有:
HCl+NaOH═NaCl+H2O
1 1
0.5mol x
则有:1:1═0.5mol:x
解得:x═0.5mol.
设反应掉0.4molFeCl3消耗消耗的NaOH物质的量为ymol,则有:
FeCl3+3NaOH═Fe(OH)3↓+3NaCl
1 3
0.2mol y
则有:1:3=0.2mol:y
解得:y═0.6mol
设反应掉0.6molAlCl3消耗的NaOH物质的量为zmol,生成Al(OH)3↓+zmol则有:
AlCl3+3NaOH═Al(OH)3↓+3NaCl
1 3 1
0.3mol y z
则有:3:1=0.3 mol:y
解得:y=1.1mol;z═0.3mol
所以,加入氢氧化钠溶液将原溶液中的FeCl3、AlCl3、HCl,全部反应完毕时,共消耗2mol.
再加入NaOH就与生成的Al(OH)3反应.
设反应掉0.3molAl(OH)3消耗的NaOH物质的量为nmol,则有:
Al(OH)3+NaOH═NaAlO2+2H2O
1 1
0.3mol n
则有:1:1═0.3 mol:n
解得:n=0.3mol.
结合反应现象及反应的量的关系,画出生成沉淀的物质的量随加入的NaOH的物质的量的关系图.
故答案为:
 向FeCl3、AlCl3的混合溶液中逐滴加入NaOH溶液分别发生如下反应:
向FeCl3、AlCl3的混合溶液中逐滴加入NaOH溶液分别发生如下反应:
AlCl3+3NaOH═Al(OH)3↓+3NaCl,FeCl3+3NaOH═Fe(OH)3↓+3NaCl,
Al(OH)3+NaOH═NaAlO2+2H2O根据反应方程式的关系得出先生成氢氧化铝、和氢氧化铁两种沉淀,体现在图象上为a点时,加入的氢氧化钠与溶液中的FeCl3、AlCl3刚好完全反应,即a点沉淀为Fe(OH)3、Al(OH)3,
故答案为:Fe(OH)3、Al(OH)3;
(2)根据图象的关系,结合反应方程式AlCl3+3NaOH═Al(OH)3↓+3NaCl,FeCl3+3NaOH═Fe(OH)3↓+3NaCl,向溶液加入3mol氢氧化钠时将,溶液中的FeCl3、AlCl3和NaOH刚好完全反应,生成Al(OH)3、Fe(OH)3沉淀,再加氢氧化钠3.6mol时,沉淀的量保持不变,又发生
Al(OH)3+NaOH═NaAlO2+2H2O,到达b点时沉淀全部为Fe(OH)3,则有:
设a点时Al(OH)3的物质的量为x mol,
Al(OH)3+NaOH═NaAlO2+2H2O
1 1
x mol (3.6-3)mol
则有:1:1=x mol:(3.6-3)mol
解得:x=0.6(mol),
设与原混合溶液中AlCl3反应的NaOH的物质的量为y mol,
AlCl3+3NaOH═Al(OH)3↓+3NaCl
3 1
y mol 0.6mol
则有:3:1=y mol:0.6 mol
解得:y=1.8(mol),
设原混合溶液中FeCl3的物质的量为z mol,
FeCl3+3NaOH═Fe(OH)3↓+3NaCl
1 3
z mol (3-1.8)mol
则有:1:3=z mol:(3-1.8)mol,
解得:z=0.4(mol),
故原混合液中FeCl3的物质的量浓度为0.4mol/0.1L=4mol/L,
故答案为:4mol/L;
(3)根据取原溶液50mL,加入0.5mol盐酸得到新溶液,其中的成分有:FeCl3、AlCl3、HCl,向其中加入NaOH溶液时,先发生HCl+NaOH═NaCl+H2O反应,当将HCl反应完后,在发生与FeCl3、AlCl3的生成沉淀,方程式为:AlCl3+3NaOH═Al(OH)3↓+3NaCl,FeCl3+3NaOH═Fe(OH)3↓+3NaCl,
完全反应后又发生反应 Al(OH)3+NaOH═NaAlO2+2H2O.
设50mL原溶液中FeCl3、AlCl3的物质的量分别为:0.2mol、0.3mol,
设中和0.5molHCl消耗的NaOH物质的量为xmol,则有:
HCl+NaOH═NaCl+H2O
1 1
0.5mol x
则有:1:1═0.5mol:x
解得:x═0.5mol.
设反应掉0.4molFeCl3消耗消耗的NaOH物质的量为ymol,则有:
FeCl3+3NaOH═Fe(OH)3↓+3NaCl
1 3
0.2mol y
则有:1:3=0.2mol:y
解得:y═0.6mol
设反应掉0.6molAlCl3消耗的NaOH物质的量为zmol,生成Al(OH)3↓+zmol则有:
AlCl3+3NaOH═Al(OH)3↓+3NaCl
1 3 1
0.3mol y z
则有:3:1=0.3 mol:y
解得:y=1.1mol;z═0.3mol
所以,加入氢氧化钠溶液将原溶液中的FeCl3、AlCl3、HCl,全部反应完毕时,共消耗2mol.
再加入NaOH就与生成的Al(OH)3反应.
设反应掉0.3molAl(OH)3消耗的NaOH物质的量为nmol,则有:
Al(OH)3+NaOH═NaAlO2+2H2O
1 1
0.3mol n
则有:1:1═0.3 mol:n
解得:n=0.3mol.
结合反应现象及反应的量的关系,画出生成沉淀的物质的量随加入的NaOH的物质的量的关系图.
故答案为:



