优质解答
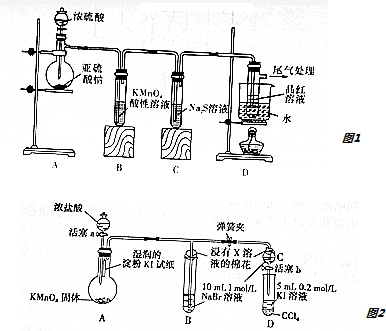
Ⅰ.图1分析可知:装置A中浓硫酸和亚硫酸钠反应生成二氧化硫,具有还原性,通过高锰酸钾溶液使之褪色,二氧化硫也有氧化性,可以和硫化钠发生反应,生成硫单质沉淀,最后二氧化硫气体通入装置D中的品红试液,品红褪色,剩余气体进行尾气处理,
(1)装置A中盛放浓硫酸仪器名称是分液漏斗,装置C中发生的现象是生成淡黄色沉淀,实验分析可知二氧化硫中硫元素化合价居于中间价态,既具有氧化性也具有还原性,特征性质是漂白性,装置B证明二氧化硫的还原性,装置C证明二氧化硫的氧化性,装置D证明二氧化硫的漂白性,选择acd,
故答案为:分液漏斗;试管中出现淡黄色沉淀;acd;
(2)二氧化硫是酸性氧化物和氢氧化钠溶液反应生成亚硫酸钠或亚硫酸钠或二者混合物,当通入二氧化硫至溶液显中性时,结合溶液中电荷守恒为:c(H+)+c(Na+)=c(OH-)+2c(SO32-)+c(HSO3-),当通入二氧化硫至溶液显中性时,此时溶液中c(Na+)=2c(SO32-)+c(HSO3-),
故答案为:2c(SO32-)+c(HSO3-);
Ⅱ.用如图2所示装置验证卤素单质氧化性的相对强弱,装置A中生成氯气,烧瓶上端湿润的碘化钾淀粉试纸变蓝色,进入装置B中的溴化钠溶液呈橙红色,氯气氧化溴离子为溴单质,打开弹簧夹,打开活塞a,殚簧夹,滴加浓盐酸,当B和C中的溶液变为黄色时,夹紧弹簧夹,当B中溶液由黄色变为棕红色时,关闭活塞a,
(3)BC中棉花团的作用是吸收剩余的氯气,用氢氧化钠溶液,Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:NaOH;
(4)装置A中产生氯气是高锰酸钾溶液和浓盐酸反应生成氯化锰、氯化钾、氯气和水,反应的化学方程式为:2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8H2O,
故答案为:2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8H2O;
(5)过程Ⅲ当B中溶液由黄色变为棕红色时,关闭活塞a,实验目的是确认C中的黄色溶液中无氯气排除氯气对溴置换碘实验的干扰,
故答案为:确认C中的黄色溶液中无氯气排除氯气对溴置换碘实验的干扰;
设计实验证明:氧化性强弱:Cl2>Br2>Fe3+,取溴化亚铁溶液少许于试管中滴加2-3滴KSCN溶液,逐滴加入氯水,溶液出现红色时,加入四氯化碳振荡,四氯化碳层无明显变化,继续滴加氯水至过量,继续振荡静置,四氯化碳层变橙红色,据此判断氧化性强弱,具体步骤为:取溴化亚铁溶液少许于试管中滴加2-3滴KSCN溶液,逐滴加入氯水,溶液出现红色时,加入四氯化碳振荡,四氯化碳层无明显变化,继续滴加氯水至过量,继续振荡静置,四氯化碳层变橙红色,则说明氧化性强弱为:Cl2>Br2>Fe3+,
故答案为:取溴化亚铁溶液少许于试管中滴加2-3滴KSCN溶液,逐滴加入氯水,溶液出现红色时,加入四氯化碳振荡,四氯化碳层无明显变化,继续滴加氯水至过量,继续振荡静置,四氯化碳层变橙红色,则说明氧化性强弱为:Cl2>Br2>Fe3+;
Ⅰ.图1分析可知:装置A中浓硫酸和亚硫酸钠反应生成二氧化硫,具有还原性,通过高锰酸钾溶液使之褪色,二氧化硫也有氧化性,可以和硫化钠发生反应,生成硫单质沉淀,最后二氧化硫气体通入装置D中的品红试液,品红褪色,剩余气体进行尾气处理,
(1)装置A中盛放浓硫酸仪器名称是分液漏斗,装置C中发生的现象是生成淡黄色沉淀,实验分析可知二氧化硫中硫元素化合价居于中间价态,既具有氧化性也具有还原性,特征性质是漂白性,装置B证明二氧化硫的还原性,装置C证明二氧化硫的氧化性,装置D证明二氧化硫的漂白性,选择acd,
故答案为:分液漏斗;试管中出现淡黄色沉淀;acd;
(2)二氧化硫是酸性氧化物和氢氧化钠溶液反应生成亚硫酸钠或亚硫酸钠或二者混合物,当通入二氧化硫至溶液显中性时,结合溶液中电荷守恒为:c(H+)+c(Na+)=c(OH-)+2c(SO32-)+c(HSO3-),当通入二氧化硫至溶液显中性时,此时溶液中c(Na+)=2c(SO32-)+c(HSO3-),
故答案为:2c(SO32-)+c(HSO3-);
Ⅱ.用如图2所示装置验证卤素单质氧化性的相对强弱,装置A中生成氯气,烧瓶上端湿润的碘化钾淀粉试纸变蓝色,进入装置B中的溴化钠溶液呈橙红色,氯气氧化溴离子为溴单质,打开弹簧夹,打开活塞a,殚簧夹,滴加浓盐酸,当B和C中的溶液变为黄色时,夹紧弹簧夹,当B中溶液由黄色变为棕红色时,关闭活塞a,
(3)BC中棉花团的作用是吸收剩余的氯气,用氢氧化钠溶液,Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:NaOH;
(4)装置A中产生氯气是高锰酸钾溶液和浓盐酸反应生成氯化锰、氯化钾、氯气和水,反应的化学方程式为:2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8H2O,
故答案为:2KMnO4+16HCl(浓)=2MnCl2+5Cl2↑+2KCl+8H2O;
(5)过程Ⅲ当B中溶液由黄色变为棕红色时,关闭活塞a,实验目的是确认C中的黄色溶液中无氯气排除氯气对溴置换碘实验的干扰,
故答案为:确认C中的黄色溶液中无氯气排除氯气对溴置换碘实验的干扰;
设计实验证明:氧化性强弱:Cl2>Br2>Fe3+,取溴化亚铁溶液少许于试管中滴加2-3滴KSCN溶液,逐滴加入氯水,溶液出现红色时,加入四氯化碳振荡,四氯化碳层无明显变化,继续滴加氯水至过量,继续振荡静置,四氯化碳层变橙红色,据此判断氧化性强弱,具体步骤为:取溴化亚铁溶液少许于试管中滴加2-3滴KSCN溶液,逐滴加入氯水,溶液出现红色时,加入四氯化碳振荡,四氯化碳层无明显变化,继续滴加氯水至过量,继续振荡静置,四氯化碳层变橙红色,则说明氧化性强弱为:Cl2>Br2>Fe3+,
故答案为:取溴化亚铁溶液少许于试管中滴加2-3滴KSCN溶液,逐滴加入氯水,溶液出现红色时,加入四氯化碳振荡,四氯化碳层无明显变化,继续滴加氯水至过量,继续振荡静置,四氯化碳层变橙红色,则说明氧化性强弱为:Cl2>Br2>Fe3+;