工业烟气通常含有二氧化硫,在排放前需经脱硫处理.如图是两种常用脱硫工艺中含硫物质的转化路径(部分产物已略).请回答下列问题:(1)反应Ⅰ的化学方程式是 .(2)反应Ⅱ所属的基本反应类型是 ,CaSO3中Ca、S、O元素的质量比是 .(3)已知原料NaOH的价格为2.9元/kg、Ca(OH)2的价格为0.36元/kg.两种工艺中,处理相同质量的SO2,双碱法所需的原料成本更低,其原因是 .
2019-04-20
工业烟气通常含有二氧化硫,在排放前需经脱硫处理.如图是两种常用脱硫工艺中含硫物质的转化路径(部分产物已略).请回答下列问题:
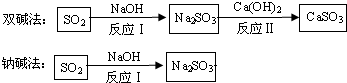
(1)反应Ⅰ的化学方程式是 ___.
(2)反应Ⅱ所属的基本反应类型是 ___,CaSO3中Ca、S、O元素的质量比是 ___.
(3)已知原料NaOH的价格为2.9元/kg、Ca(OH)2的价格为0.36元/kg.两种工艺中,处理相同质量的SO2,双碱法所需的原料成本更低,其原因是 ___.

(1)反应Ⅰ的化学方程式是 ___.
(2)反应Ⅱ所属的基本反应类型是 ___,CaSO3中Ca、S、O元素的质量比是 ___.
(3)已知原料NaOH的价格为2.9元/kg、Ca(OH)2的价格为0.36元/kg.两种工艺中,处理相同质量的SO2,双碱法所需的原料成本更低,其原因是 ___.