某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为2%的氢氧化钠溶液进行中和,如图所示.(1)恰好完全中和废水中的盐酸所用的氢氧化钠溶液的质量是g.(2)废水中盐酸的溶质质量分数是多少?
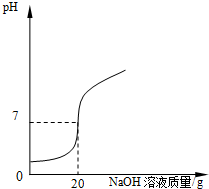 某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为2%的氢氧化钠溶液进行中和,如图所示.
某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为2%的氢氧化钠溶液进行中和,如图所示.
(1)恰好完全中和废水中的盐酸所用的氢氧化钠溶液的质量是______g.
(2)废水中盐酸的溶质质量分数是多少?
2019-04-20
 某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为2%的氢氧化钠溶液进行中和,如图所示.
某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用质量分数为2%的氢氧化钠溶液进行中和,如图所示.(1)恰好完全中和废水中的盐酸所用的氢氧化钠溶液的质量是______g.
(2)废水中盐酸的溶质质量分数是多少?