优质解答
| (1)间接; (2)B; (3)设需要x千克氢氧化钙才能完全中和,则 Ca(OH) 2 +2HCl=CaCl 2 +2H 2 O 74 2×36.5 x 1.0×10 6 kg×0.00365% 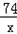 = =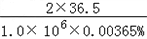 解得:x=37kg 答:需要37千克氢氧化钙才能完全中和. |
| (1)间接; (2)B; (3)设需要x千克氢氧化钙才能完全中和,则 Ca(OH) 2 +2HCl=CaCl 2 +2H 2 O 74 2×36.5 x 1.0×10 6 kg×0.00365% 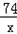 = =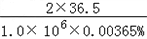 解得:x=37kg 答:需要37千克氢氧化钙才能完全中和. |