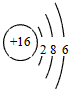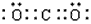下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题: (1)写出⑧的原子结构示意图。(2)④、⑤、⑥的原子半径由大到小的顺序为(用元素符号回答)。 (3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(用化学式回答)。(4)②与④形成的原子个数比为1:2化合物的电子式为。(5)⑥的单质与①、④、⑤三种元素形成化合物的水溶液反应的离子方程式为:。(6)②的最高价氧化物的熔沸点低于⑦的最高价氧化物的熔沸点,原因是。(7)⑤元素与⑨元素形成的化合物中,化学键
2019-04-21
| 下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题: |
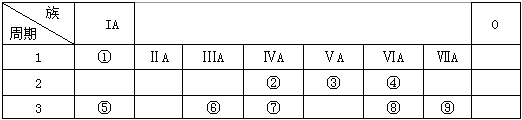 |
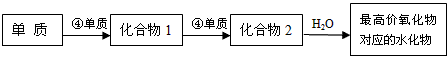
| (1)写出⑧的原子结构示意图________________。 (2)④、⑤、⑥的原子半径由大到小的顺序为______________________(用元素符号回答)。 (3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是__________________(用化学式回答)。 (4)②与④形成的原子个数比为1:2化合物的电子式为________________。 (5)⑥的单质与①、④、⑤三种元素形成化合物的水溶液反应的离子方程式为:__________________。 (6)②的最高价氧化物的熔沸点低于⑦的最高价氧化物的熔沸点,原因是________________。 (7)⑤元素与⑨元素形成的化合物中,化学键类型为________________,高温灼烧该化合物时,火焰呈 ________色。 (8)在②、③、⑦、⑧单质中,符合下列转化关系的是:________________(填元素符号)。 |
 |