某化学研究小组通过上网查找资料发现N2的制取有如下两种方法:方法a:加热条件下利用NH3还原CuO制得纯净的N2和活性铜粉.方法b:将空气缓慢通入灼热的铜粉制得较纯净的N2.现实验室提供如下几种装置来制取N2.(1)若按方法a制取N2时,需要的氨气用生石灰和浓氨水作原料制取,则宜采用上述装置(填序号)作为发生器,该发生装置中发生反应的化学方程式为.要制取并收集纯净的N2(允许含有少量水蒸气),还需使用到上述装置(按气流从左到右的流向顺序列出)(填序号).(2)若按方法b制取N2,用装置E将空气缓慢通入(填
 某化学研究小组通过上网查找资料发现N2的制取有如下两种方法:
某化学研究小组通过上网查找资料发现N2的制取有如下两种方法:
方法a:加热条件下利用NH3还原CuO制得纯净的N2和活性铜粉.
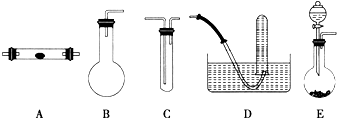
方法b:将空气缓慢通入灼热的铜粉制得较纯净的N2.现实验室提供如下几种装置来制取N2.
(1)若按方法a制取N2时,需要的氨气用生石灰和浓氨水作原料制取,则宜采用上述装置______(填序号)作为发生器,该发生装置中发生反应的化学方程式为______.要制取并收集纯净的N2(允许含有少量水蒸气),还需使用到上述装置(按气流从左到右的流向顺序列出)______(填序号).
(2)若按方法b制取N2,用装置E将空气缓慢通入______(填“A”、“B”或“C”)反应器,该反应器内可观察到的现象是______,该反应的化学方程式为
2019-05-30
 某化学研究小组通过上网查找资料发现N2的制取有如下两种方法:
某化学研究小组通过上网查找资料发现N2的制取有如下两种方法:方法a:加热条件下利用NH3还原CuO制得纯净的N2和活性铜粉.
方法b:将空气缓慢通入灼热的铜粉制得较纯净的N2.现实验室提供如下几种装置来制取N2.
(1)若按方法a制取N2时,需要的氨气用生石灰和浓氨水作原料制取,则宜采用上述装置______(填序号)作为发生器,该发生装置中发生反应的化学方程式为______.要制取并收集纯净的N2(允许含有少量水蒸气),还需使用到上述装置(按气流从左到右的流向顺序列出)______(填序号).
(2)若按方法b制取N2,用装置E将空气缓慢通入______(填“A”、“B”或“C”)反应器,该反应器内可观察到的现象是______,该反应的化学方程式为
O2+2Cu
CuO
| ||
O2+2Cu
CuO
.
| ||