优质解答
| (1)AB (2)3Cu+2N 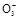 +8H + +8H +  3Cu 2+ +2NO↑+4H 2 O 3Cu 2+ +2NO↑+4H 2 O |
| (1)n(H 2 SO 4 )="0.1" L×18 mol·L -1 ="1.8" mol,根据反应:2H 2 SO 4 (浓)+Cu  CuSO 4 +SO 2 ↑+2H 2 O,硫酸完全反应,将有0.9 mol的H 2 SO 4 被还原为SO 2 气体,体积为20.16 L,但实际上随反应的进行,硫酸浓度变小,不能与铜反应,则生成的SO 2 体积小于20.16 L,可能是AB。 CuSO 4 +SO 2 ↑+2H 2 O,硫酸完全反应,将有0.9 mol的H 2 SO 4 被还原为SO 2 气体,体积为20.16 L,但实际上随反应的进行,硫酸浓度变小,不能与铜反应,则生成的SO 2 体积小于20.16 L,可能是AB。(2)加入NaNO 3 后,剩余的稀硫酸与N 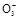 相当于存在稀硝酸,发生稀硝酸与Cu的反应: 相当于存在稀硝酸,发生稀硝酸与Cu的反应:3Cu+2N 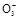 +8H + +8H +  3Cu 2+ +2NO↑+4H 2 O。 3Cu 2+ +2NO↑+4H 2 O。 |
| (1)AB (2)3Cu+2N 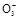 +8H + +8H +  3Cu 2+ +2NO↑+4H 2 O 3Cu 2+ +2NO↑+4H 2 O |
| (1)n(H 2 SO 4 )="0.1" L×18 mol·L -1 ="1.8" mol,根据反应:2H 2 SO 4 (浓)+Cu  CuSO 4 +SO 2 ↑+2H 2 O,硫酸完全反应,将有0.9 mol的H 2 SO 4 被还原为SO 2 气体,体积为20.16 L,但实际上随反应的进行,硫酸浓度变小,不能与铜反应,则生成的SO 2 体积小于20.16 L,可能是AB。 CuSO 4 +SO 2 ↑+2H 2 O,硫酸完全反应,将有0.9 mol的H 2 SO 4 被还原为SO 2 气体,体积为20.16 L,但实际上随反应的进行,硫酸浓度变小,不能与铜反应,则生成的SO 2 体积小于20.16 L,可能是AB。(2)加入NaNO 3 后,剩余的稀硫酸与N 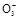 相当于存在稀硝酸,发生稀硝酸与Cu的反应: 相当于存在稀硝酸,发生稀硝酸与Cu的反应:3Cu+2N 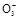 +8H + +8H +  3Cu 2+ +2NO↑+4H 2 O。 3Cu 2+ +2NO↑+4H 2 O。 |