食盐是一种重要的化工原料.请回答下列问题.(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤.[溶解]→[操作Ⅰ]→[蒸发]①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和.②在蒸发过程中,待时,停止加热,利用余热将滤液蒸干.(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制.流程如图.①加入稍过量的Na2CO3溶液,除了能除去粗盐中的含有CaCl2外,它还有一个作用是(用化学方程式表示).②通过操作Ⅲ所得滤液中的溶质有(用化学式表示).(3)已
2019-11-27
食盐是一种重要的化工原料.请回答下列问题.
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤.[溶解]→[操作Ⅰ]→[蒸发]
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和___.
②在蒸发过程中,待___时,停止加热,利用余热将滤液蒸干.
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制.流程如图.
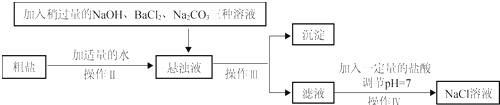
①加入稍过量的Na2CO3溶液,除了能除去粗盐中的含有CaCl2外,它还有一个作用是___(用化学方程式表示).
②通过操作Ⅲ所得滤液中的溶质有___(用化学式表示).
(3)已知:20℃时氯化钠的溶解度为36g.若有溶质质量分数为10%的氯化钠不饱和溶液100kg,要将其变成20℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是___.
(1)请完善实验室除去粗盐中泥沙等难溶性杂质的实验步骤.[溶解]→[操作Ⅰ]→[蒸发]
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和___.
②在蒸发过程中,待___时,停止加热,利用余热将滤液蒸干.
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制.流程如图.

①加入稍过量的Na2CO3溶液,除了能除去粗盐中的含有CaCl2外,它还有一个作用是___(用化学方程式表示).
②通过操作Ⅲ所得滤液中的溶质有___(用化学式表示).
(3)已知:20℃时氯化钠的溶解度为36g.若有溶质质量分数为10%的氯化钠不饱和溶液100kg,要将其变成20℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是___.