利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.请回答下列问题:(1)已知COCl2分子的结构式为,则COCl2分子内含有(填标号);A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3 个σ键、1个π键(2)Fe(CO)5中铁的化合价为0,写出Fe元素基态原子的价电子排布式;Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可以判断Fe(CO)5晶体类型为.(3)Fe(CO)5在一定条件下发生分解反应
2019-11-27
利用CO可以合成化工原料COCl2、配合物Fe(CO)5等.请回答下列问题:
(1)已知COCl2分子的结构式为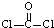 ,则COCl2分子内含有______(填标号);
,则COCl2分子内含有______(填标号);
A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3 个σ键、1个π键
(2)Fe(CO)5中铁的化合价为0,写出Fe元素基态原子的价电子排布式______;
Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可以判断Fe(CO)5晶体类型为______.
(3)Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是______.
(4)与CO分子互为等电子体的分子和离子各写出1种,分别为______和______(填化学式).
(1)已知COCl2分子的结构式为
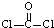 ,则COCl2分子内含有______(填标号);
,则COCl2分子内含有______(填标号);A.4个σ键 B.2个σ键、2个π键 C.2个σ键、1个π键 D.3 个σ键、1个π键
(2)Fe(CO)5中铁的化合价为0,写出Fe元素基态原子的价电子排布式______;
Fe(CO)5常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂.据此可以判断Fe(CO)5晶体类型为______.
(3)Fe(CO)5在一定条件下发生分解反应:Fe(CO)5=Fe(s)+5CO,反应过程中,断裂的化学键只有配位键,形成的化学键是______.
(4)与CO分子互为等电子体的分子和离子各写出1种,分别为______和______(填化学式).
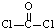 ,分子中含有2个单键和1个双键,则COCl2分子内含有3个σ键、1个π键,
,分子中含有2个单键和1个双键,则COCl2分子内含有3个σ键、1个π键,