下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题:(1)9种元素中,原子半径最小的是.(2)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是.(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是.(4)元素③的氢化物的电子式为;该氢化物常温下和⑨的氢化物两者反应的实验现象是,上述反应得到一种盐,属于化合物(填离子或共价).检验该盐溶液中阳离子存在的方法是(5)⑤和⑧两元素可形成化合物,该化合物灼烧时火焰颜色为色,用电子式表示该化合物的形成过程.(6)写出⑥的最高价氧化物与
2019-04-21
下表为元素周期表的一部分,请参照元素①-⑨在表中的位置,用化学用语回答下列问题: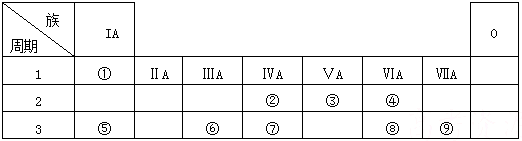
(1)9种元素中,原子半径最小的是______.
(2)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是______.
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______.
(4)元素③的氢化物的电子式为______;该氢化物常温下和⑨的氢化物两者反应的实验现象是______,上述反应得到一种盐,属于______化合物(填离子或共价).检验该盐溶液中阳离子存在的方法是______
(5)⑤和⑧两元素可形成化合物,该化合物灼烧时火焰颜色为______色,用电子式表示该化合物的形成过程______.
(6)写出⑥的最高价氧化物与⑤的最高价氧化物对应水化物反应的离子方程式______.
(7)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为______(填序号).
A.MnO2 B.FeCl3 C.Na2SO3 D.KMnO4.

(1)9种元素中,原子半径最小的是______.
(2)④、⑤、⑥三种元素形成的简单离子中,离子半径最大的是______.
(3)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是______.
(4)元素③的氢化物的电子式为______;该氢化物常温下和⑨的氢化物两者反应的实验现象是______,上述反应得到一种盐,属于______化合物(填离子或共价).检验该盐溶液中阳离子存在的方法是______
(5)⑤和⑧两元素可形成化合物,该化合物灼烧时火焰颜色为______色,用电子式表示该化合物的形成过程______.
(6)写出⑥的最高价氧化物与⑤的最高价氧化物对应水化物反应的离子方程式______.
(7)由表中两种元素的原子按1:1组成的常见液态化合物的稀溶液易被催化分解,可使用的催化剂为______(填序号).
A.MnO2 B.FeCl3 C.Na2SO3 D.KMnO4.
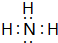 ,⑨的氢化物为HCl,二者反应生成氯化铵固体而产生白烟,氯化铵属于离子化合物,检验该盐溶液中阳离子存在的方法是:取少量溶液于试管中,加入浓的氢氧化钠溶液微热,在试管口放一片湿润的红色石蕊试纸,若试纸变蓝则含有氨根离子,
,⑨的氢化物为HCl,二者反应生成氯化铵固体而产生白烟,氯化铵属于离子化合物,检验该盐溶液中阳离子存在的方法是:取少量溶液于试管中,加入浓的氢氧化钠溶液微热,在试管口放一片湿润的红色石蕊试纸,若试纸变蓝则含有氨根离子, ,
,