CH3COOH为常见的弱酸,在工业生产和生活中有广泛的应用. (1)常温下中和100mL pH=3的CH3COOH溶液和1L pH=4的CH3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1V2 (填“>”、“=”或“<”),中和后所得溶液中离子浓度由大到小的顺序为.(2)用0.1000mol•L-1NaOH溶液滴定20.00mL某未知浓度的醋酸溶液,滴定曲线如图所示.其中①点所示溶液中c(CH3COO-)=2c(CH3COOH),③点
2019-05-30
CH3COOH为常见的弱酸,在工业生产和生活中有广泛的应用.
(1)常温下中和100mL pH=3的CH3COOH溶液和1L pH=4的CH3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1___V2 (填“>”、“=”或“<”),中和后所得溶液中离子浓度由大到小的顺序为___.
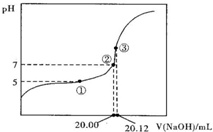
(2)用0.1000mol•L-1NaOH溶液滴定20.00mL某未知浓度的醋酸溶液,滴定曲线如图所示.其中①点所示溶液中c(CH3COO-)=2c(CH3COOH),
③点所示溶液中存在:c(CH3COO-)+c(CH3COOH)═c(Na+).则CH3COOH的电离平衡常数Ka=___,CH3COOH的实际浓度为___.

(1)常温下中和100mL pH=3的CH3COOH溶液和1L pH=4的CH3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1___V2 (填“>”、“=”或“<”),中和后所得溶液中离子浓度由大到小的顺序为___.
(2)用0.1000mol•L-1NaOH溶液滴定20.00mL某未知浓度的醋酸溶液,滴定曲线如图所示.其中①点所示溶液中c(CH3COO-)=2c(CH3COOH),
③点所示溶液中存在:c(CH3COO-)+c(CH3COOH)═c(Na+).则CH3COOH的电离平衡常数Ka=___,CH3COOH的实际浓度为___.