氢氧化钠溶液与稀盐酸发生中和反应时观察不到明显现象,为了确定其反应是否发生,某班同学设计了不同的实验方案进行探究.(1)按照如图1的方式,向烧杯中逐滴滴入盐酸至过量的过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是;(2)按照如图2的方案完成实验:其中②处不可以选择的试剂是(填序号,下同),若①②颠倒顺序,仍能证明盐酸与氢氧化钠发生了反应,这种试剂是;A.Zn粒 B.AgNO3溶液 C.石蕊试液 D.Na2CO3溶液(3)下列方案中,能证明氢氧化钠溶液与稀盐酸发
2019-06-27
氢氧化钠溶液与稀盐酸发生中和反应时观察不到明显现象,为了确定其反应是否发生,某班同学设计了不同的实验方案进行探究.
(1)按照如图1的方式,向烧杯中逐滴滴入盐酸至过量的过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是___;
(2)按照如图2的方案完成实验:其中②处不可以选择的试剂是___(填序号,下同),若①②颠倒顺序,仍能证明盐酸与氢氧化钠发生了反应,这种试剂是___;
A.Zn粒 B.AgNO3溶液 C.石蕊试液 D.Na2CO3溶液
(3)下列方案中,能证明氢氧化钠溶液与稀盐酸发生了反应的是___(填序号);
A.用pH试纸测定氢氧化钠溶液的pH值,然后向其中滴加稀盐酸,pH逐渐减少,最终小于7
B.用温度计测试氢氧化钠溶液滴加稀盐酸前后的温度,温度明显上升
C.向一定的氢氧化钠溶液中滴加硫酸铜溶液,有蓝色沉淀生成,再加稀盐酸后沉淀消失
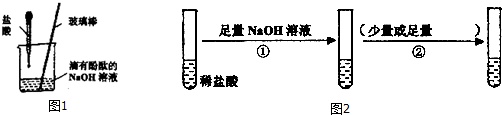
(1)按照如图1的方式,向烧杯中逐滴滴入盐酸至过量的过程中,能够说明盐酸与氢氧化钠发生了化学反应的实验现象是___;
(2)按照如图2的方案完成实验:其中②处不可以选择的试剂是___(填序号,下同),若①②颠倒顺序,仍能证明盐酸与氢氧化钠发生了反应,这种试剂是___;
A.Zn粒 B.AgNO3溶液 C.石蕊试液 D.Na2CO3溶液
(3)下列方案中,能证明氢氧化钠溶液与稀盐酸发生了反应的是___(填序号);
A.用pH试纸测定氢氧化钠溶液的pH值,然后向其中滴加稀盐酸,pH逐渐减少,最终小于7
B.用温度计测试氢氧化钠溶液滴加稀盐酸前后的温度,温度明显上升
C.向一定的氢氧化钠溶液中滴加硫酸铜溶液,有蓝色沉淀生成,再加稀盐酸后沉淀消失
