氯化亚铜是一种无机精细化工产品,实验室用蚀刻废液(主要含CuCl2、HCl等)制备CuCl的实验流程如下.(1)滤渣1的主要成分为;还原时生成[CuCl2]-的离子方程式为.(2)加水时发生反应的离子方程式为.过滤时用的硅酸盐质仪器除烧杯外还有.滤液2的用途是.(3)用稀盐酸洗涤的目的是.
2019-11-23
氯化亚铜是一种无机精细化工产品,实验室用蚀刻废液(主要含CuCl2、HCl等)制备CuCl的实验流程如下.
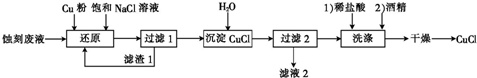
(1)滤渣1的主要成分为___;还原时生成[CuCl2]-的离子方程式为___.
(2)加水时发生反应的离子方程式为___.过滤时用的硅酸盐质仪器除烧杯外还有___.滤液2的用途是___.
(3)用稀盐酸洗涤的目的是___.

(1)滤渣1的主要成分为___;还原时生成[CuCl2]-的离子方程式为___.
(2)加水时发生反应的离子方程式为___.过滤时用的硅酸盐质仪器除烧杯外还有___.滤液2的用途是___.
(3)用稀盐酸洗涤的目的是___.