乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:已知:①氯化钙可与乙醇形成CaCl2•6C2H5OH②有关有机物的沸点:试剂乙醚乙醇乙酸乙酸乙酯沸点/℃34.778.511877.1③2CH3CH2OH浓硫酸140℃CH3CH2OCH2CH3+H2OI.制备过程:装置如图所示,A中放有浓硫酸,B中放有9.5mL无水乙醇和6mL冰醋酸,D中放有饱和碳酸钠溶液.(1)写出乙酸与乙醇发生酯化反应的化学方程式CH3COOH+C2H5OH浓硫酸△CH3COOC2H5+H2OC
 乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
已知:①氯化钙可与乙醇形成CaCl2•6C2H5OH
②有关有机物的沸点:
③2CH3CH2OH
CH3CH2OCH2CH3+H2O
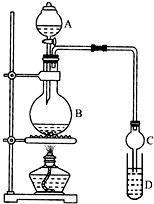
I.制备过程:装置如图所示,A中放有浓硫酸,B中放有9.5mL无水乙醇和6mL冰醋酸,D中放有饱和碳酸钠溶液.
(1)写出乙酸与乙醇发生酯化反应的化学方程式
(2)浓硫酸对该乙酸乙酯合成反应的影响是:______.
(3)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是______(填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL
(4)设计简单实验证明饱和碳酸钠溶液是否起到了吸收乙酸的作用:______.
(5)实验过程中发现两层之间出现了白色固体,请用化学方程式表示形成原因:______
Ⅱ.提纯方法
①将D中混合液转入分液漏斗进行分液.
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤.有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物.
③将粗产物蒸馏,收集77.1℃的馏分,得到纯净干燥的乙酸乙酯.
(6)第①步分液时,选用的两种玻璃仪器的名称分别是______、______.
(7)第②步中用饱和食盐水、饱和氯化钙溶液、最后用水洗涤,分别主要洗去粗产品中的______,______,______.
2019-11-23
 乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:
乙酸乙酯是一种用途广泛的精细化工产品.某课外小组设计实验室制取并提纯乙酸乙酯的方案如下:已知:①氯化钙可与乙醇形成CaCl2•6C2H5OH
②有关有机物的沸点:
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
| 浓硫酸 |
| 140℃ |
I.制备过程:装置如图所示,A中放有浓硫酸,B中放有9.5mL无水乙醇和6mL冰醋酸,D中放有饱和碳酸钠溶液.
(1)写出乙酸与乙醇发生酯化反应的化学方程式
CH3COOH+C2H5OH
CH3COOC2H5+H2O
| 浓硫酸 |
| △ |
CH3COOH+C2H5OH
CH3COOC2H5+H2O
.| 浓硫酸 |
| △ |
(2)浓硫酸对该乙酸乙酯合成反应的影响是:______.
(3)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是______(填入正确选项前的字母)
A.25mL B.50mL C.250mL D.500mL
(4)设计简单实验证明饱和碳酸钠溶液是否起到了吸收乙酸的作用:______.
(5)实验过程中发现两层之间出现了白色固体,请用化学方程式表示形成原因:______
Ⅱ.提纯方法
①将D中混合液转入分液漏斗进行分液.
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤.有机层倒入一干燥的烧瓶中,用无水硫酸镁干燥,得粗产物.
③将粗产物蒸馏,收集77.1℃的馏分,得到纯净干燥的乙酸乙酯.
(6)第①步分液时,选用的两种玻璃仪器的名称分别是______、______.
(7)第②步中用饱和食盐水、饱和氯化钙溶液、最后用水洗涤,分别主要洗去粗产品中的______,______,______.