纳米氧化铝在陶瓷材料、电子工业、生物医药等方面有广阔的应用前景,它可通过硫酸铝铵晶体热分解得到.制备硫酸铝铵晶体的实验流程如下:回答下列问题:(1)上述流程中加入氨水后产生的沉淀是(填化学式).(2)检验上述流程中“过滤”后杂质是否除尽所用的试剂是(填化学式).(3)上述流程中,“分离”所包含的操作依次为:蒸发浓缩、、过滤、洗涤、干燥.(4)己知:硫酸铝铵晶体的化学式为Al2(NH4)4(S04)n•24H20,相对分子质量为906.取4.53g硫酸铝铵晶体加热分解,加热过程中,固体质量随温度的变化如图所
2020-02-08
纳米氧化铝在陶瓷材料、电子工业、生物医药等方面有广阔的应用前景,它可通过硫酸铝铵晶体热分解得到.制备硫酸铝铵晶体的实验流程如下: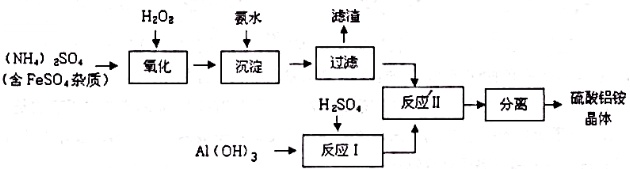
回答下列问题:
(1)上述流程中加入氨水后产生的沉淀是___(填化学式).
(2)检验上述流程中“过滤”后杂质是否除尽所用的试剂是___(填化学式).
(3)上述流程中,“分离”所包含的操作依次为:蒸发浓缩、___、过滤、洗涤、干燥.
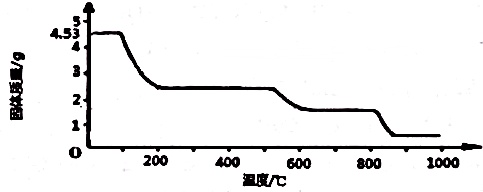
(4)己知:硫酸铝铵晶体的化学式为Al2(NH4)4(S04)n•24H20,相对分子质量为906.取4.53g硫酸铝铵晶体加热分解,加热过程中,固体质量随温度的变化如图所示.最终剩余固体为Al2O3,计算所得氧化铝的质量___.

回答下列问题:
(1)上述流程中加入氨水后产生的沉淀是___(填化学式).
(2)检验上述流程中“过滤”后杂质是否除尽所用的试剂是___(填化学式).
(3)上述流程中,“分离”所包含的操作依次为:蒸发浓缩、___、过滤、洗涤、干燥.
(4)己知:硫酸铝铵晶体的化学式为Al2(NH4)4(S04)n•24H20,相对分子质量为906.取4.53g硫酸铝铵晶体加热分解,加热过程中,固体质量随温度的变化如图所示.最终剩余固体为Al2O3,计算所得氧化铝的质量___.
