硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料.三氯化硼 (BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂.查阅资料:①BCl3的沸点为12.5℃,熔点为-107.3℃;②2B+6HCl═2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应.设计实验:某同学设计如图所示装置利用氯气和单质硼反应制备三氯化硼:请回答下列问题:(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,而且不需要加热,两个反应的产物中锰的价态相同.写出高锰酸
2019-12-02
硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料.三氯化硼 (BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂.
查阅资料:①BCl3的沸点为12.5℃,熔点为-107.3℃;②2B+6HCl═2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应.
设计实验:某同学设计如图所示装置利用氯气和单质硼反应制备三氯化硼:
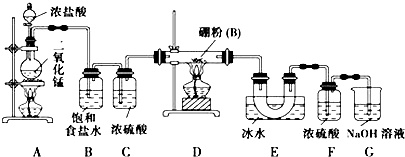
请回答下列问题:
(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,而且不需要加热,两个反应的产物中锰的价态相同.写出高锰酸钾固体粉末与浓盐酸反应的离子方程式:___.
(2)E装置的作用是___.如果拆去B装置,可能的后果是___.
(3)实验中可以用一个盛装___ (填试剂名称)的干燥管代替F和G装置,使实验更简便.
(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式:___;
(5)为了顺利完成实验,正确的操作是___ (填序号)
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(6)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓___ (填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉.
查阅资料:①BCl3的沸点为12.5℃,熔点为-107.3℃;②2B+6HCl═2BCl3↑+3H2↑;③硼与铝的性质相似,也能与氢氧化钠溶液反应.
设计实验:某同学设计如图所示装置利用氯气和单质硼反应制备三氯化硼:

请回答下列问题:
(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,而且不需要加热,两个反应的产物中锰的价态相同.写出高锰酸钾固体粉末与浓盐酸反应的离子方程式:___.
(2)E装置的作用是___.如果拆去B装置,可能的后果是___.
(3)实验中可以用一个盛装___ (填试剂名称)的干燥管代替F和G装置,使实验更简便.
(4)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式:___;
(5)为了顺利完成实验,正确的操作是___ (填序号)
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(6)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓___ (填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉.