2019-04-21
下表是部分短周期元素的信息,用化学用语回答下列问题。
| 元素 |
D | M | G | E | ||||||||||||
| 性质 结构 信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远。 | 氢化物常温下呈液态,M的双原子阴离子有18个电子 | 原子核外的M层比L层少2个电子。 | +3价阳离子的核外电子排布与氖原子相同。 |
(1)元素A在周期表中的位置 。B的某种核素中中子数比质子数多1,则表示该核素的原子符号为 。
(2)写出钙与M原子个数比为1:2化合物的电子式
钙与A原子个数比为1:2化合物含有的化学键类型(填离子键、共价键或非极性键)
。
(3)M2-、D+、G2-离子半径大小顺序是 > > (用离子符号回答)。
 (4)由A、B、M及氢四种原子构成的分子A2H5BM2,既可以和盐酸反应又可以和氢氧化钠溶液反应,写出A2H5BC2的名称 。
(4)由A、B、M及氢四种原子构成的分子A2H5BM2,既可以和盐酸反应又可以和氢氧化钠溶液反应,写出A2H5BC2的名称 。
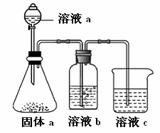
(5)某同学设计实验证明A、B、F的非金属性强弱关系。
① 溶液a和b分别为 , 。
② 溶液c中的离子方程式为 。
(6)将0.5 mol D2M2投入100 mL 3 mol/L ECl3溶液中,转移电子的物质的量为 。
(7)工业上冶炼E,以石墨为电极,阳极产生的混合气体的成分为 。