I.硫酸铜是一种应用极其广泛的化工原料.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4•5H2O)的生产流程示意图:胆矾和石膏在不同温度下的溶解度(g/100g水)见下表. 温度(℃) 20 40 60 80 100 石膏 0.32 0.26 0.15 0.11 0.07 胆矾 32 44.6 61.8 83.8 114请回答下列问题:(1)红棕色滤渣的主要成分是;(2)写出浸出过程中生成硫酸铜的化学方程式;(3)操作I的操作温度应该控制在℃左右;
2019-11-27
I.硫酸铜是一种应用极其广泛的化工原料.以下是某工厂用含铁废铜为原料生产胆矾(CuSO4•5H2O)的生产流程示意图:
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表.
请回答下列问题:
(1)红棕色滤渣的主要成分是______;
(2)写出浸出过程中生成硫酸铜的化学方程式______;
(3)操作I的操作温度应该控制在______℃左右;
(4)从溶液中分离出硫酸铜晶体的操作II应为______、洗涤、干燥;
(5)取样检验是为了确认Fe3+是否除净.有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液;
方案二:径向层析→喷KSCN溶液
①你认为上述两种方案设计更合理的是______;
②指出你认为不合理的方案存在的问题______;
(6)反应产物中的NO可以循环使用,用化学方程式表示循环使用的方案______.
II.(12分)复印机使用的墨粉主要成份是Fe3O4,图是氧化沉淀法生产Fe3O4的工艺: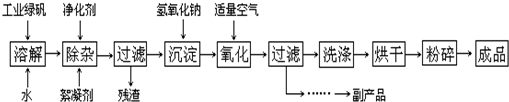
已知:
①工业绿矾中FeSO4的含量为52.5%,其中的杂质不参与反应;
②Fe(OH)2+2Fe(OH)3═Fe3O4•4H2O
请回答下列问题:
(1)铁的常见氧化物有______;
(2)Fe3O4与盐酸反应的化学方程式是:______,检验反应后的溶液中含Fe3+的方法:______;
(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是:______;
(4)生产中可获得的副产品是______,提取该副产品的操作顺序是:______(填写序号)
a.过滤 b.加热浓缩 c.冷却 d.结晶 e.洗涤
(5)在生产过程中,若工业绿矾的投料速率是12.16kg/h,为使产品较纯,鼓入空气的速率应为______m3/h(假设反应在标准状态下进行,空气中O2占20%).

胆矾和石膏在不同温度下的溶解度(g/100g水)见下表.
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
(1)红棕色滤渣的主要成分是______;
(2)写出浸出过程中生成硫酸铜的化学方程式______;
(3)操作I的操作温度应该控制在______℃左右;
(4)从溶液中分离出硫酸铜晶体的操作II应为______、洗涤、干燥;
(5)取样检验是为了确认Fe3+是否除净.有同学设计了以下两种方案,在实验室分别对所取样品按下列方案进行操作:
方案一:取样于试管→滴加KSCN溶液;
方案二:径向层析→喷KSCN溶液
①你认为上述两种方案设计更合理的是______;
②指出你认为不合理的方案存在的问题______;
(6)反应产物中的NO可以循环使用,用化学方程式表示循环使用的方案______.
II.(12分)复印机使用的墨粉主要成份是Fe3O4,图是氧化沉淀法生产Fe3O4的工艺:

已知:
①工业绿矾中FeSO4的含量为52.5%,其中的杂质不参与反应;
②Fe(OH)2+2Fe(OH)3═Fe3O4•4H2O
请回答下列问题:
(1)铁的常见氧化物有______;
(2)Fe3O4与盐酸反应的化学方程式是:______,检验反应后的溶液中含Fe3+的方法:______;
(3)在工艺流程中,通入适量空气“氧化”时的化学方程式是:______;
(4)生产中可获得的副产品是______,提取该副产品的操作顺序是:______(填写序号)
a.过滤 b.加热浓缩 c.冷却 d.结晶 e.洗涤
(5)在生产过程中,若工业绿矾的投料速率是12.16kg/h,为使产品较纯,鼓入空气的速率应为______m3/h(假设反应在标准状态下进行,空气中O2占20%).