二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,它极易与水反应.为在实验室合成S2Cl2,某化学研究性学习小组查阅有关资料,有如下两种反应原理:①CS2+3Cl2 95-100℃ CCl4+S2Cl2;②2S+Cl2 50-60℃ S2Cl2.几种物质的熔、沸点数据如下表所示: 物质 S CS2 CCl
2019-12-02
二氯化二硫(S2Cl2)在工业上用于橡胶的硫化,它极易与水反应.为在实验室合成S2Cl2,某化学研究性学习小组查阅有关资料,有如下两种反应原理:
①CS2+3Cl2
CCl4+S2Cl2;②2S+Cl2
S2Cl2.
几种物质的熔、沸点数据如下表所示:
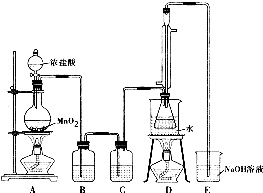
(1)如图装置(部分夹持仪器已略去)D到E有一处不够完善,清你提出改进的措施:___;利用改进后的正确装置进行实验,反应原理应采用上述两个反应中的___(填①或②).
(2)B中盛放饱和氯化钠溶液,其作用是___;C中盛放试剂的名称是___.
(3)D装置中水从冷凝管___端通入(选填“上”或“下”).反应结束后,从D装置锥形瓶内的混合物中分离出产品的操作为___(填名称).
(4)S2Cl2与水反应产生无色、有刺激性气味的气体,并有黄色沉淀生成,该反应的化学万程式为___.
①CS2+3Cl2
| 95-100℃ |
| |
| 50-60℃ |
| |
几种物质的熔、沸点数据如下表所示:
| 物质 | S | CS2 | CCl4 | S2Cl2 |
| 沸点/℃ | 445 | 47 | 77 | 137 |
| 熔点/℃ | 113 | -109 | -23 | -77 |
(2)B中盛放饱和氯化钠溶液,其作用是___;C中盛放试剂的名称是___.
(3)D装置中水从冷凝管___端通入(选填“上”或“下”).反应结束后,从D装置锥形瓶内的混合物中分离出产品的操作为___(填名称).
(4)S2Cl2与水反应产生无色、有刺激性气味的气体,并有黄色沉淀生成,该反应的化学万程式为___.
