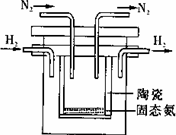
合成氨是化学固氮的主要途径.中学教材介绍的合成氨技术称为哈伯法,是德国科学家哈伯于1905年发明的,其反应原理是:N 2 (g)+3H 2 (g) 2NH 3 (g); △H=-92 . 4kJ/mol(该反应热数据在25℃、101kPa条件下测得),他因此获得了1918年诺贝尔化学奖.试分析和回答下列问题: (1) 在合成氨工业中,常选择下列反应条件,其中可以用勒夏特别原理解释的是 . [ ] A. 采用20—50
2019-06-24
|
|
| ||||||||||||||||||||||||
 2NH 3 (g);
2NH 3 (g);