化学•选修3:物质结构与性质硫及其化合物广泛存在于自然界中,并被人们广泛利用.回答下列问题:(1)当基态原子的电子吸收能量后,电子会发生,某处于激发态的S原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为.(2)苯酚()中羟基被硫羟基取代生成苯硫酚(),苯硫酚的酸性比苯酚的酸性强,原因是.(3)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH).①甲硫醇中C-S键与S-H键的键角(填“小于”或“等于”)180°,甲硫醇分子中C原子杂化轨道类型是,S原子杂化轨道类型
2019-05-22
化学•选修3:物质结构与性质
硫及其化合物广泛存在于自然界中,并被人们广泛利用.回答下列问题:
(1)当基态原子的电子吸收能量后,电子会发生___,某处于激发态的S原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为___.
(2)苯酚(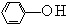 )中羟基被硫羟基取代生成苯硫酚(
)中羟基被硫羟基取代生成苯硫酚(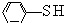 ),苯硫酚的酸性比苯酚的酸性强,原因是___.
),苯硫酚的酸性比苯酚的酸性强,原因是___.
(3)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH).
①甲硫醇中C-S键与S-H键的键角___(填“小于”或“等于”)180°,甲硫醇分子中C原子杂化轨道类型是___,S原子杂化轨道类型是___.
②甲醇和甲硫醇的部分物理性质如下表:
甲醇和甲硫醇在熔沸点和水溶性方面性质差异的原因是___.
(4)科学家通过X射线推测胆矾结构示意图1:
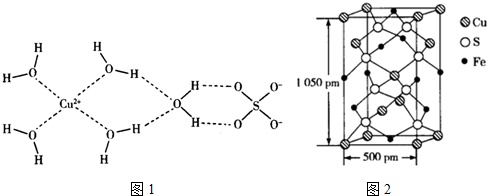
其中含有___个配位键,___个氢键.
(5)某化合物由S、Fe、Cu三种元素组成,其晶胞结构如图2所示(1pm=10-10cm),该晶胞上下底面为正方形,侧面与底面垂直,则该晶体的密度ρ=___g•cm-3(保留三位有效数字).
硫及其化合物广泛存在于自然界中,并被人们广泛利用.回答下列问题:
(1)当基态原子的电子吸收能量后,电子会发生___,某处于激发态的S原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为___.
(2)苯酚(
 )中羟基被硫羟基取代生成苯硫酚(
)中羟基被硫羟基取代生成苯硫酚(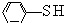 ),苯硫酚的酸性比苯酚的酸性强,原因是___.
),苯硫酚的酸性比苯酚的酸性强,原因是___.(3)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH).
①甲硫醇中C-S键与S-H键的键角___(填“小于”或“等于”)180°,甲硫醇分子中C原子杂化轨道类型是___,S原子杂化轨道类型是___.
②甲醇和甲硫醇的部分物理性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 水溶液 |
| 甲醇 | -97 | 64.7 | 互溶 |
| 甲硫醇 | -123 | 6.8 | 不溶 |
(4)科学家通过X射线推测胆矾结构示意图1:

其中含有___个配位键,___个氢键.
(5)某化合物由S、Fe、Cu三种元素组成,其晶胞结构如图2所示(1pm=10-10cm),该晶胞上下底面为正方形,侧面与底面垂直,则该晶体的密度ρ=___g•cm-3(保留三位有效数字).