研究和控制化学反应条件有重要意义.①同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以制取氧气,同学们可以选择下列图1中的(选填编号)装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是,因此加热不适合用于双氧水制取氧气.②同学们还想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间. 实验 30%双氧水的质量(g) 加入的水的体积(m
2019-12-02
研究和控制化学反应条件有重要意义.
①同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以制取氧气,同学们可以选择下列图1中的___(选填编号)装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是___,因此加热不适合用于双氧水制取氧气.
②同学们还想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
Ⅰ. 取用二氧化锰的仪器是图2中的___(选填编号).
Ⅱ.写出上述反应的化学反应方程式___.
Ⅲ.本实验中收集氧气选用的装置有___(选填编号).
Ⅳ.实验2中双氧水溶质质量分数为___.
Ⅴ.实验3中,加入的二氧化锰质量为___g.
Ⅵ.相同条件下,实验3产生氧气的速率最快,说明___.
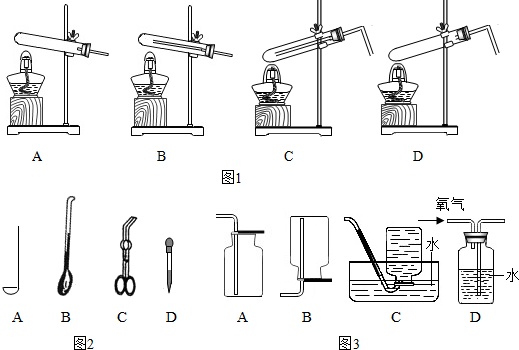
①同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以制取氧气,同学们可以选择下列图1中的___(选填编号)装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是___,因此加热不适合用于双氧水制取氧气.
②同学们还想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | ___ | 67 |
Ⅱ.写出上述反应的化学反应方程式___.
Ⅲ.本实验中收集氧气选用的装置有___(选填编号).
Ⅳ.实验2中双氧水溶质质量分数为___.
Ⅴ.实验3中,加入的二氧化锰质量为___g.
Ⅵ.相同条件下,实验3产生氧气的速率最快,说明___.
