GB/T 4789.9-2008
基本信息
标准号: GB/T 4789.9-2008
中文名称:食品卫生微生物学检验 空肠弯曲菌检验
标准类别:国家标准(GB)
英文名称:Microbiological examination of food hygiene - Examination of campylobacter jejuni
标准状态:已作废
发布日期:1984-12-25
实施日期:2009-03-01
作废日期:2015-05-01
下载格式:pdf zip

标准分类号
标准ICS号: 数学、自然科学>>微生物学>>07.100.30
中标分类号:医药、卫生、劳动保护>>卫生>>C53食品卫生
出版信息
出版社:中国标准出版社
书号:155066·1-36049
页数:14页
标准价格:31.0
出版日期:2009-03-01
相关单位信息
首发日期:1984-12-25
起草人:蒋原、刘秀梅、祝长青、郭云昌、廖兴广、栾军、袁宝君、程苏云、田静
起草单位:江苏出入境检验检疫局、中国疾病预防控制中心营养与食品安全所等
归口单位:卫生部
提出单位:中华人民共和国卫生部
发布部门:中华人民共和国卫生部 中国国家标准化管理委员会
主管部门:卫生部
标准简介
本标准代替GB/T 4789.9-2003《食品卫生微生物学检验 空肠弯曲菌检验》。
本标准规定了食品中空肠弯曲菌的检验方法。
本标准适用于食品和食源性疾病样品中空肠弯曲菌的检验。
本标准与GB/T 4789.9-2003相比主要修改如下:
———删除了规范性引用文件;
———修改并完善了操作步骤;
———增加了弯曲菌的酶联荧光免疫检验方法作为筛选检验法;
———删除了生物分型、血清分型、菌株保存与注意事项的内容;
———增加了附录A“培养基与试剂”。
标准图片预览




标准内容
1CS 07. 100. 30
中华人民具和国国家标准
GB/T 4789.9---2008
代替 GB/T 4789.92003
食品卫生微生物学检验
空肠弯曲菌检验
Microbiological examination of food hygieneExamination of Campylobacter jejuni2008-11-21 发布
中华人民共和国卫生部
中国国家标准化管理委员会
2009-03-01实施
中华人民共和国
国家标雁
食品卫生微生物学检验
空肠弯曲菌检验
GB/T 4789. 9—2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网证 spc. net. cn
电话:68523916
68517548
中国标准出版社案皇岛印刷厂印刷各地新华书店经销
并本 880×1230
印张 1学数 25T字
2009年3月第-版
2009年3月第一次印刷
书号:155066·1-36049定价16.00元如有印装差错
由本社发行中心调换此内容来自唯久标准下载网
侵权必究
版权专有
举报电话:(010)68533533
GB/T 4789.9—2008
本标准的第-法修改采用ISO10272-1:2006《食品和动物饲料的微生物学检验和计数弯曲菌的等同方法第1部分:检验方法》(Microbiology of food and aninal feeding stuffs--Harixontal tuethatlfor dctectian axd euimeration of Campylobacter spp. Part l Detcetion mcthod).本标准的第一法与ISO10272-1:2006的主要区别如F:删除了规范性引用文件、术语和定义、检验原理;一增加并完菩了各类样品的处理、增菌培养;.-增加了Skirruw琼脂与0.1%蛋白陈水。本标雅代替(G3/T4789.9—2003《食品卫生微生物学检验空肠弯曲菌检验》。本标准与GB/T4789.9—2003相比主要修改如下:删除了规范性引用文件;
修改并完善了操作步骤;
—…-增加了弯曲菌的酶联荧光免疫检验方法作为筛选检验法:删除了生物分型、血清分型、菌株保存与注意事项的内容;-增加了附录A“培养基与试剂”。本标准的附录A为规范性附录。
本标准由中华人民共和国卫生部提出并归口。本标准由中华人民共和国卫生部负责解释。本标准负责起草单位:中华人民北和国江苏出人境检验检疫局、中国疾病预防控制中心营养与食品安全所。
本标准参加起草单位:河南省疾病预防控制中心、江苏省疾病预防控制中心、浙江省疾病预防控制中心。
本标准主要起草人:蒋原、刘秀梅、祝长青、郭云昌、廖兴广、森军、袁宝君、程苏云、田静。本标准所代替标准的历次版本发布情况为:GB4789.91984、GB/T4789.9—1994、CB/T4789.9—2003。I
1范围
食品卫生微生物学检验
空肠弯曲菌检验
本标准规定了食品中空肠弯曲菌(Campyfobacterjejuni)的检验方法。本标准适用于食品和食源性疾病样品中空肠弯曲菌的检验。2设备和材料
除微作物实验室常规灭菌与培养设备外,其他设备与材料如下:2.1 冰箱:2℃~8℃。
2.2恒温培养箱:25 ℃士1 ,36 ℃±1 ℃,42 ℃±1 ℃2.3恒温振荔培养箱:36℃上1℃,42℃11℃。2. 4 水装置:36 ℃±1 ℃,100 ℃。2.5微需氧培养装置:提供微需氧条件(5%氧气、10%二氧化碳和85%氮气)。2.6均质器。
2.7电于犬平:感量 0.1 g。
2.8过滤装置及滤膜(0.22μm,0.45μm)。2.9显微镜:10×~100×,有相差功能2.10离心机:离心力20000×g。2.11全自动微生物鉴定系统(VITEK 2)\)2.12全自动酶联爽光免疫分析仪(VIDAS或miniVIDAS)\)。3培养基和试剂
3.1Bolton肉汤:按第A.1章规定。3.2改良 CCD(mCCD)琼脂:按第 A. 2 章规定。3.3哥伦比亚琼脂:按第A.3章规定。3.4布氏肉汤:按第A.4章规定。3.5氧化酶试剂:按第A,5 章规定。3. 6马尿酸钠水解试剂:按第 A. 6 章规定。3.7MucllerHinton琼脂:按第A.7章规定。3.8吲哚乙酸酯纸片:按第A.8章规定。3,9Skirraw琼脂:按第 A.9章规定。3.100.1%蛋白陈水:按第A.10章规定。3.11CFA显色平板。
3. 12 1 mol/L 碳酸氨钠(NaHCO,)波。3.133%过氧化氢溶液。
3.14API Campy生化鉴定试剂盒\。3.15VITEK 2 NH 生化鉴定卡”。GB/T 4789.9—2008
1)由法国生物梅里埃(bioMerieux)公司提供的产品的商品名。给出这-信息是为厂方他本标准的使用者,并不表示对该产品的认可。如果其他等效产品具有相尚的效果,则可使用这些等效的产品、1
全品伙伴网
GB/T 4789.9-2008
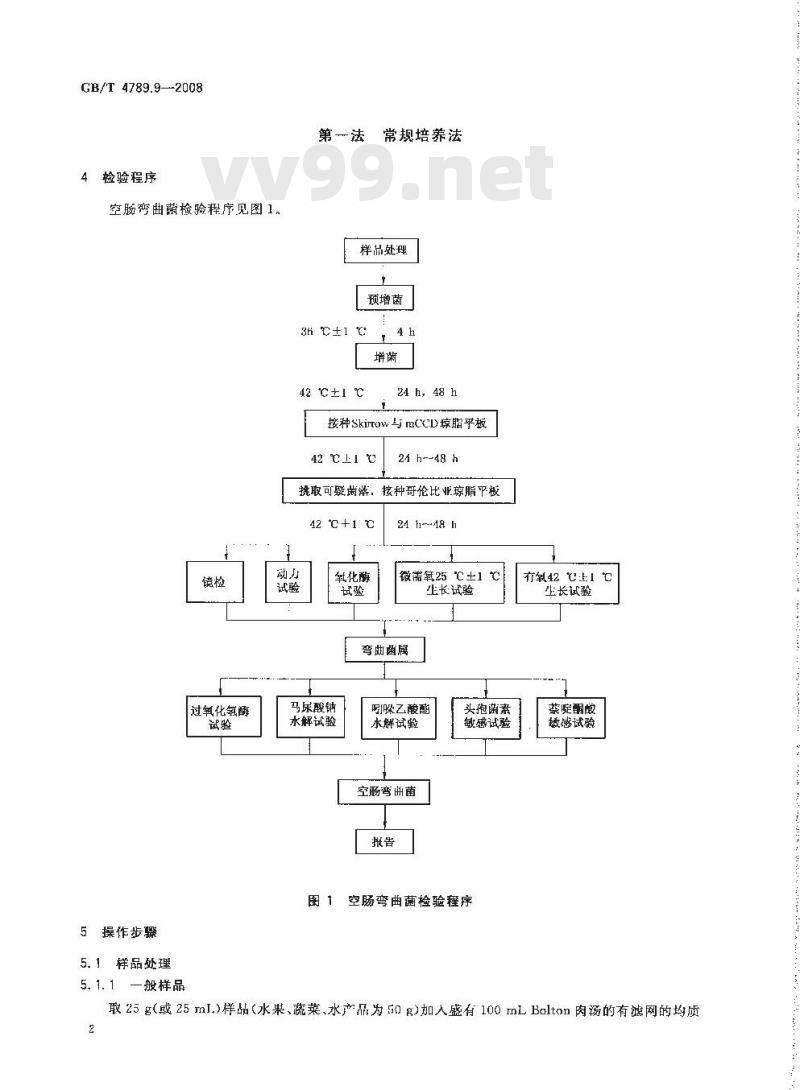
4检验程序
空肠驾曲菌检验程序见图1
过氧化氢酶
5操作步骤
5.1样品处理
5.1. 1一般样品
第一法
常规培养法
样品处理
预增菌
36 C±1
42 ±1 ℃
24 h,48 h
种skinow与mccD琼脂乎板
24 h--48 h
挑取可疑菌落,接种哥伦比业琼脂平板42 ℃+1 c
氧化酶
24 h~-48 h
微端氧25℃±1
生长试验
弯曲菌属
马尿酸钠
水解试验
吲哚乙酸酯
水解试验
空肠湾曲菌
头孢菌素
敏感试验
空肠弯曲菌检验程序
有氧42℃1
生长试验
啶酮酸
敏感试验
取25g(或25mI.)样品(水果、蔬菜、水产品为50g)加人盛有100mLBalton肉汤的有滤网的均质2
http:/
ww.foodmate.net
GB/T 4789.9—2008
袋中(无滤网的均质袋可使用无菌纱过滤),用拍击式图质器均质1min-~2mit或加入盛有100mLBolton肉汤的哟质杯中,以8 000 t/min~10 000 r/min均质1 min~2min,经滤网或无菌纱布过滤。将滤液进行培养。
5.1.2鲜乳、冰淇淋、奶酪等
取50g样品加人盛有50ml.0.1%蛋白陈水的有滤网均质袋中,必要时调整pH值至7.2士0.2.用拍击式均质器均质15s~-30s,将滤液以2000×g离心30min后弃去上清,用10tnLBol1an肉汤悬浮沉淀(尽避免带人油层),再转移至90mL不含抗生素的olton肉汤进行培养。5. 1. 3贝类
取至少12个带壳样品,除去外充后将所有内容物放到均质袋中,用拍击式均质器均质1min~2 min,取25 g样品于 225 mL Boltal 肉汤中(1 : 1 稀释),再转移 25 mL~225 mL Bolton 肉汤中(1:100稀释),将1:10和1100稀释的Bolton肉汤向时进行培养。5. 1.4蛋黄液或蛋浆
取25g(或25mL)样品于125mLBolton肉汤中并搅勾(1:6稀释),再转移25ml.~100mLBalton肉汤中并搅勺(1:30稀释),同时将1:6和1:30稀释的Bolton肉进行培养。5.1.5整禽等样品
用200ml.0.1%的蛋白水充分冲洗样品的内外部,并振荡2min~-3min,经无菌纱布过滤至250mL离心管中,16C00×g离心15min后弃去上清,用10ml.0.1%蛋白陈水忌浮沉淀,吸取3ml.~100 ml.I3alton肉汤中进行培养。5.1.6需表面涂拭检测的样品
无菌棉签涂布样品表面(面积为50cm~100cm),将棉签头剪落到100tmLBalton肉汤中进行培。
5. 1.7水样
将41.的水(对了氯处理的水,在过滤前每升水中加人5mL1mal/L硫代硫酸钠溶液)经0.15μm滤膜过滤,将滤膜浸没在oomL Boltun肉汤中进行培养。5.2预增菌与增菌
在微需氧条件下,以100z/mi的振荡速度,36℃士1℃培养4h。必要时测定增菌液的pH值并调整至7.2±0.2。42℃+1℃继续培养48h5.3分离
将24h增菌液、48h增菌液以及相应的1:50稀释液分别划线接种于Skirrow与mCCD琼胎平板上,微需氧条件下42℃士1℃培养24h~48h。另外,可同时选择使用CFA显色乎板。观察24h培养与48h培养的琼脂平板上的菌落形态。mCCD琼脂平板上的可疑菌落通常有光泽,潮湿、扇平,呈扩散生长的倾向,直径约为1tmm~-2mmSkirruw琼脂平板l的可疑菌落为灰色、巅平、润有光泽,呈沿接种线向外扩散的倾问;有些可疑菌落常皇分散凸起的单个菌落,直径约为1mm2mm,边缘整齐、发亮。CFA显色平板上的可疑菌落为红色、突起、湿润,菌落直径约为2mm~3mm,近缘有一圈红色的透明环,中间有:-个圆形的、不透明、颜色较深的红色小点的荫落。5.4鉴定
5.4.1鸾曲菌属的鉴定
挑取5个或更多的可凝菌落接种到哥伦比亚琼脂平板上,微需氧条件下42℃士1℃培养21h~48h,按照5.4.1.1~5.4.1.5进行鉴定,结果符合表1的可疑菌落确定为弯曲菌属。3
GB/T4789.9—2008
形态观察
动力观察
氧化醇实验
微需氧条件下25 ℃±1℃生长试验有氧条件下42℃±1℃生长实验
有些菌株的形态不典型。
b有些菌株的运动不明显。
5.4.1.1形态观察
表1弯曲菌属的监定
弯曲菌属性
莹兰氏阴性,菌体弯曲如小点状,两荫体的未端相接时呈S形、蝶旋状或海鸥展翅状”
圣现螺放状运动
不生长
不生长
挑可疑菌落进行革兰氏染色,镜检。5.4.1.2动力观察
挑取可疑菌落用1mI.布氏肉荡悬浮,用相养显微镜观察运动状态。5.4.1.3氧化酶试验
用铂/铱接种环或玻璃棒挑取可疑菌落至氧化悔试剂润湿的滤纸上,如果在10s内出现紫红色、紫罗兰或深蓝色为阳性。
5.4.1.4微需氧条件下25℃±1℃生长试验挑取可疑菌落,接种到哥伦比亚琼脂平板上,微需氧条件下25℃十1℃焙养44h土1h,观察细菌生长情况。
5.4. 1.5有氧条件下42℃±1℃生长试验挑取可疑菌落,接种到哥伦比亚琼脂平板上,有氧条件下42℃土1℃培养44h十4h,观察细菌生长情况。
5.4.2空肠弯曲菌的监定
5.4.2.1过化氢酶试验:挑取菌落,加到于净玻片上的3%过氧化氢溶液中,如果在30s内出现气泡则判定结果为阳性。
5.4.2.2马尿酸钠水解试验:挑取菌落,加到感有0.4mL1%马尿酸钠的试管中制成菌悬液。混合均匀后在36℃士1℃水浴放置2h或36℃士1℃培养箱中放置1h。沿着试管壁缓缓加入0.2mL节-酮溶液,不要振荡,在36℃±1℃的水浴或培养箱中放置10 min后判读结果。若出现深紫色则为阳性;若出现淡紫色或没有颜色变化则为阴性。5.4.2.3吲哚乙酸酯水解试验:挑取菌落至吲哚乙酸酯纸片上,再滴加一滴灭菌水。如果吲哚乙酸醋水解,则在5min~10min内出现深蓝色;若无颜色变化则没有发生水解。5.4.2.4药物敏感性试验(可选择):挑取菌落,在布氏肉汤中制备成浓度为0.5McFarlad的菌悬液,再用布氏肉汤制备1=10的稀释液,在5%MuellerHinton琼脂平板上进行涂布,静置5min后去除多余液体,将平板在36℃土1C培养箱中放置10rnin进行1燥。将头孢需素(30g)和萘啶酮(30μg)药敏纸片放在琼脂表面。将平板在微需氧条件下36℃土1℃培养22h土2h。如果细菌紧贴着纸片牛长则为有抗性;如果纸片周围山现不同程度的细菌抑制生长则为敏感。空肠弯曲菌的鉴定结果见表2。品成伴网ht
过氧化氢酶试验
马尿酸盐水解试验
吲哚乙酸酯水解试验
头孢菌素敏感试验
紫啶酮酸敏感试验
表 2 空肠弯曲菌的鉴定
空肠弯曲菌
(C. ieiu)
注+阴性;一阴性;S敏感;R抗性。结晰弯曲菌
(C. cpit)
空肠弯曲菌和结肠弯曲菌对禁啶酮酸的耐药性呈现出增长趋势。b 海鸥弯曲菌的不同菌株,分别表现为敏感或抗性。海鹏弯曲菊
tr. tari)
GB/T 4789.9—2008
乌·肾萨拉弯曲菌
(C. μpsatiensis)
-或微弱
5.4.2.5对于确定为弯帕属的菌落,可使用APICampy生化鉴定试剂盒或VITEK2NII牛化鉴定卡来替代5.4.2.1~5.4.2.4的鉴定,具体操作按照产品说明书进行。5. 5结果报告
综合以上试验结果,报告检样单位中检出空肠弯曲菌或未检出空肠弯曲菌。第二法全自动酶联荧光免疫分析仪筛选法6原理
弯曲菌的酶联荧光免疫筛选法是在全自动酶联荧光免疫分析仪1.进行的双抗体夹心酶联荧光免疫检验方法。固相容器(SPR)用抗弯曲菌抗体包被,各种试剂均封闭在试剂条内。煮沸过的增菌肉汤加人试条孔,在特定时间内样本在SPR内外反复循坏,使得弯曲菌抗原与包被在SPR内部的弯曲菌抗体结合,洗涤去除未结合的其他成分。接着标记有碱性磷酸酶的抗体与固定在SPR壁上的弯曲菌抗原相结合,洗去未结合的抗体标记物。结合在SPR壁上的碱性磷酸酶将催化底物磷酸4-甲基伞型物转变成具有荧光的4-甲基伞形酮,以450nm波长处检测荧光强度,出仪器分析后得出检验结果。7仪器
mini VIDAS或 VIDAS.
8试剂
8.1弯曲菌试剂条(VIDASCAM)。
8.2校正液:纯化灭活的弯曲菌抗原标准溶液。8.3阳性对照。
8.4阴性对照。
8.5 MLE卡.
操作步骤
9.1增菌液处理
取lmL24h培养的Bolton增菌液加人试替中,100℃水浴15min。剩余增菌液继续培养至48h,5
GB/T4789.9—2008
9.2仪器操作
9.2.1输入MLE卡信息
每个试剂盆在使用之前,首先要用试剂盒中的MLE卡向仪器输入试剂规格(或曲线数据)。每盒试剂只需输人次。
9. 2. 2 校正
在输入MI.-卡信息后,使用试剂盒内的校正液进行校正,校正应做双份测试。以后存14d进行次校正。
9.3检测
取出试剂条,待恢复至室温后进行样本编号。建立工作表格,输人样本编号,分别吸取500uL阴性、阳性对照和样本(冷却至室温)加人到试剂条样本孔中央。依照屏幕提示,将VIDAS CAM试剂条放入仪器的相应位置。所有分析过程由仪器自动完成。9.4结果报告
9.4.1检测值(X)是样品的相对荧光值(RFV.)与标准溶液的相对荧光值(RFV。)的比值,见式(1)X = RFV,
若检测值0.10,则检测结果为阴性;若检测值含0.10,则检测结果为阳性。(1)
9.4.2检测结果阴性,可直接报告检验单位中末检出空肠曲菌。检测结果阳性的样品,应按照5.3~5.4对剩余增菌液进行确认并报告。A,1Bolton肉汤(Bnltonhroth)
A. 1. 1 基础培养基
A.1.1.1成分
附录A
(规范性附录)
培养基与试剂
动物组织酶解物(enzymatic:digestalanimaltissues)乳白蛋白水解物(lauctalbuinhydrolysate酵母浸膏
氯化钠
丙酮酸钠
偏亚硫酸氢钠
碳酸钠
α-酮戊二酸
A,1,1.2 制法
1 000 mL
CB/T 4789.9—2008
用水溶解基础培养基成分,如需要可使用加热促其溶解。将基础培养基分装牟合适的锥形瓶内,121 ℃灭菌 15 min-
A.1.2无菌裂解脱纤维绵羊或马血对无菌脱纤维编羊或马血通过反复冻融进行裂解或使用皂角苷进行裂解,A.1.3抗生素溶液
A. 1.3. 1 成分
头孢哌酮(cefuperazae)
万古霉素(vuncomycin)
H甲氧芋胺嘧啶乳酸盐(trimethoprim lactate)两性莓蒸B(amphotercinB)
多粘菌素B(polymyxin B)
乙醇/灭菌水(50/50,体积比)A. 1. 3. 2 制法
将上述成分溶解于乙醇/菌水混合溶液中。A. 1. 4 完全培养基
A, 1. 4. 1 成分
基础培养基(A.1.1)
无菌裂解脱纤维绵羊或马血(A.1.2)抗牛素溶液(A,1.3)
1000 mL
A, 1.4. 2 制法
当基础培养基的温度约为45℃左右时,无菌加人绵羊或乃血和抗生素溶液,混勾,将完全培养基的pH值调至7.2士0.2(25℃),将培养基无菌分装至合适的试管或锥形瓶中备用。配制的增菌液在常温下放置不得超过4h,或在4左右避光保存不得超过7d。7
合品成伴网httn
GB/T4789.9—2008
A.2改良CCi)琼脂(modiriedcharcoalcefoperazonedeoxycholateagar,mCcDA)A.2.1基础培养基
A.2.1.1成分
肉浸液
动物组织酶解物
氯化钠
酪蛋白酶解物
去氧胆酸钠
硫酸业铁
丙酮酸钠
A. 2. 1.2制法
8, 0 g~18. 0 g
1000ml
用水溶解基础培养基成分,煮沸。分装至合适的三角瓶内,121℃高压灭菌15min。A,2.2抗生紊溶液
A.2.2.1成分
头孢葡(cefoperaznne)
两性霉素B(amphotericinB)
利福平(rilatmpicin)
乙醇/灭菌水(50/50,休积比)A. 2. 2. 2 制法
将述成分溶解于乙醇/灭菌水混合溶液中。A.2.3完全培养基
A, 2. 3. 1 成分
基础培养基(A.2.1)
抗生素溶液(A.2.2)
A,2.3.2制法
1000mL
当基础培养的温度约为15℃左右时,加人抗生素溶液,混匀。将完全培养基的pH值调至7.210.2(25℃)。倾注约15mL于无菌平血中,静置至培养基凝固。使用前需预先干燥平板。t将平皿盖打开,使培养基面朝下,置于于燥箱中约30min,直到琼脂表面于燥。预先制备的平板未十燥时在室温放置不得超过4l,或在4C左右冷藏不得超过7d.A.3哥伦比亚琼脂(Columbia bloodagar)A,3.1基础培养基
A.3.1.1成分
动物组织酶解物
氯化钠
合伙伴网
8. 0 g~18.0 g
1 000 mL
A.3. 1.2 制法
GB/T4789.9—2008
将基础培养基成分溶解于水中,加热促其溶解,分装至合适的三角瓶内,121℃高压灭菌151nit。A.3.2无菌脱纤维绵羊血
无菌操作条件下,将绵羊血加入到盛有灭菌玻璃珠的容器中,振摇约10min,静置后除去附有血纤维的玻璃珠即可。
A.3.3完全培养基
A.3.3. 1组分
基础培养基(A.3.1)
无菌脱纤维绵羊血(A.3.2)
A.3.3.2制法
1000tmL
当基础培养基的温度为45℃左右时,无菌加人缔羊血,混匀。将完金培养基的pFI值调至7.2士0.2(25℃)。倾注15mL十无菌平血中,静置至培养基凝固。使用前需预先干燥平板。可将平血盖打开,使培养基面朝下,置于干爆箱中约30rin,直到琼脂表面干燥。预先制备的平板末干燥时在窄温放置不得超过 4 h,或在 4 ℃左右冷藏不得超过 7 d。A.4布氏肉汤(Brucellabroth)A.4.1成分
酪蛋白酶解物
动物组织酶解物
葡萄糖
酵母浸音
氯化钠
亚硫酸氢钠
A, 4.2制法
1 000 mL
将基础培养基成分溶解丁水中,妇需要可加热促其溶解。将高压灭菌后培养基的pH值调至7.0十0.2(25℃))。将培养基分装至合适的试管中,每管10mL,121℃高压灭菌15min,A.5氧化酶试剂(reagentforthedetectionofoxidase)A.5.1成分
四甲基对苯一胺盐酸盐(N,N.N',N'-tetramcthyl-1,4-phenylenediaminedihydrochloride)蒸馏水
A.5.2制法
使用前迅速将上述成分溶于水中。1.0g
100 mL
A.6马尿酸钠水解试剂((reagents for the detection of hydrolysis of hippurate)A.6.1马尿酸钠溶液
A.6. 1. 1 成分
马尿酸钠
磷酸盐缓冲液(PBS)组分:
氯化钠(NaC1))
磷酸氢二钠(NaHPO,·2HzO)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。
中华人民具和国国家标准
GB/T 4789.9---2008
代替 GB/T 4789.92003
食品卫生微生物学检验
空肠弯曲菌检验
Microbiological examination of food hygieneExamination of Campylobacter jejuni2008-11-21 发布
中华人民共和国卫生部
中国国家标准化管理委员会
2009-03-01实施
中华人民共和国
国家标雁
食品卫生微生物学检验
空肠弯曲菌检验
GB/T 4789. 9—2008
中国标准出版社出版发行
北京复兴门外三里河北街16号
邮政编码:100045
网证 spc. net. cn
电话:68523916
68517548
中国标准出版社案皇岛印刷厂印刷各地新华书店经销
并本 880×1230
印张 1学数 25T字
2009年3月第-版
2009年3月第一次印刷
书号:155066·1-36049定价16.00元如有印装差错
由本社发行中心调换此内容来自唯久标准下载网
侵权必究
版权专有
举报电话:(010)68533533
GB/T 4789.9—2008
本标准的第-法修改采用ISO10272-1:2006《食品和动物饲料的微生物学检验和计数弯曲菌的等同方法第1部分:检验方法》(Microbiology of food and aninal feeding stuffs--Harixontal tuethatlfor dctectian axd euimeration of Campylobacter spp. Part l Detcetion mcthod).本标准的第一法与ISO10272-1:2006的主要区别如F:删除了规范性引用文件、术语和定义、检验原理;一增加并完菩了各类样品的处理、增菌培养;.-增加了Skirruw琼脂与0.1%蛋白陈水。本标雅代替(G3/T4789.9—2003《食品卫生微生物学检验空肠弯曲菌检验》。本标准与GB/T4789.9—2003相比主要修改如下:删除了规范性引用文件;
修改并完善了操作步骤;
—…-增加了弯曲菌的酶联荧光免疫检验方法作为筛选检验法:删除了生物分型、血清分型、菌株保存与注意事项的内容;-增加了附录A“培养基与试剂”。本标准的附录A为规范性附录。
本标准由中华人民共和国卫生部提出并归口。本标准由中华人民共和国卫生部负责解释。本标准负责起草单位:中华人民北和国江苏出人境检验检疫局、中国疾病预防控制中心营养与食品安全所。
本标准参加起草单位:河南省疾病预防控制中心、江苏省疾病预防控制中心、浙江省疾病预防控制中心。
本标准主要起草人:蒋原、刘秀梅、祝长青、郭云昌、廖兴广、森军、袁宝君、程苏云、田静。本标准所代替标准的历次版本发布情况为:GB4789.91984、GB/T4789.9—1994、CB/T4789.9—2003。I
1范围
食品卫生微生物学检验
空肠弯曲菌检验
本标准规定了食品中空肠弯曲菌(Campyfobacterjejuni)的检验方法。本标准适用于食品和食源性疾病样品中空肠弯曲菌的检验。2设备和材料
除微作物实验室常规灭菌与培养设备外,其他设备与材料如下:2.1 冰箱:2℃~8℃。
2.2恒温培养箱:25 ℃士1 ,36 ℃±1 ℃,42 ℃±1 ℃2.3恒温振荔培养箱:36℃上1℃,42℃11℃。2. 4 水装置:36 ℃±1 ℃,100 ℃。2.5微需氧培养装置:提供微需氧条件(5%氧气、10%二氧化碳和85%氮气)。2.6均质器。
2.7电于犬平:感量 0.1 g。
2.8过滤装置及滤膜(0.22μm,0.45μm)。2.9显微镜:10×~100×,有相差功能2.10离心机:离心力20000×g。2.11全自动微生物鉴定系统(VITEK 2)\)2.12全自动酶联爽光免疫分析仪(VIDAS或miniVIDAS)\)。3培养基和试剂
3.1Bolton肉汤:按第A.1章规定。3.2改良 CCD(mCCD)琼脂:按第 A. 2 章规定。3.3哥伦比亚琼脂:按第A.3章规定。3.4布氏肉汤:按第A.4章规定。3.5氧化酶试剂:按第A,5 章规定。3. 6马尿酸钠水解试剂:按第 A. 6 章规定。3.7MucllerHinton琼脂:按第A.7章规定。3.8吲哚乙酸酯纸片:按第A.8章规定。3,9Skirraw琼脂:按第 A.9章规定。3.100.1%蛋白陈水:按第A.10章规定。3.11CFA显色平板。
3. 12 1 mol/L 碳酸氨钠(NaHCO,)波。3.133%过氧化氢溶液。
3.14API Campy生化鉴定试剂盒\。3.15VITEK 2 NH 生化鉴定卡”。GB/T 4789.9—2008
1)由法国生物梅里埃(bioMerieux)公司提供的产品的商品名。给出这-信息是为厂方他本标准的使用者,并不表示对该产品的认可。如果其他等效产品具有相尚的效果,则可使用这些等效的产品、1
全品伙伴网
GB/T 4789.9-2008
4检验程序
空肠驾曲菌检验程序见图1
过氧化氢酶
5操作步骤
5.1样品处理
5.1. 1一般样品
第一法
常规培养法
样品处理
预增菌
36 C±1
42 ±1 ℃
24 h,48 h
种skinow与mccD琼脂乎板
24 h--48 h
挑取可疑菌落,接种哥伦比业琼脂平板42 ℃+1 c
氧化酶
24 h~-48 h
微端氧25℃±1
生长试验
弯曲菌属
马尿酸钠
水解试验
吲哚乙酸酯
水解试验
空肠湾曲菌
头孢菌素
敏感试验
空肠弯曲菌检验程序
有氧42℃1
生长试验
啶酮酸
敏感试验
取25g(或25mI.)样品(水果、蔬菜、水产品为50g)加人盛有100mLBalton肉汤的有滤网的均质2
http:/
ww.foodmate.net
GB/T 4789.9—2008
袋中(无滤网的均质袋可使用无菌纱过滤),用拍击式图质器均质1min-~2mit或加入盛有100mLBolton肉汤的哟质杯中,以8 000 t/min~10 000 r/min均质1 min~2min,经滤网或无菌纱布过滤。将滤液进行培养。
5.1.2鲜乳、冰淇淋、奶酪等
取50g样品加人盛有50ml.0.1%蛋白陈水的有滤网均质袋中,必要时调整pH值至7.2士0.2.用拍击式均质器均质15s~-30s,将滤液以2000×g离心30min后弃去上清,用10tnLBol1an肉汤悬浮沉淀(尽避免带人油层),再转移至90mL不含抗生素的olton肉汤进行培养。5. 1. 3贝类
取至少12个带壳样品,除去外充后将所有内容物放到均质袋中,用拍击式均质器均质1min~2 min,取25 g样品于 225 mL Boltal 肉汤中(1 : 1 稀释),再转移 25 mL~225 mL Bolton 肉汤中(1:100稀释),将1:10和1100稀释的Bolton肉汤向时进行培养。5. 1.4蛋黄液或蛋浆
取25g(或25mL)样品于125mLBolton肉汤中并搅勾(1:6稀释),再转移25ml.~100mLBalton肉汤中并搅勺(1:30稀释),同时将1:6和1:30稀释的Bolton肉进行培养。5.1.5整禽等样品
用200ml.0.1%的蛋白水充分冲洗样品的内外部,并振荡2min~-3min,经无菌纱布过滤至250mL离心管中,16C00×g离心15min后弃去上清,用10ml.0.1%蛋白陈水忌浮沉淀,吸取3ml.~100 ml.I3alton肉汤中进行培养。5.1.6需表面涂拭检测的样品
无菌棉签涂布样品表面(面积为50cm~100cm),将棉签头剪落到100tmLBalton肉汤中进行培。
5. 1.7水样
将41.的水(对了氯处理的水,在过滤前每升水中加人5mL1mal/L硫代硫酸钠溶液)经0.15μm滤膜过滤,将滤膜浸没在oomL Boltun肉汤中进行培养。5.2预增菌与增菌
在微需氧条件下,以100z/mi的振荡速度,36℃士1℃培养4h。必要时测定增菌液的pH值并调整至7.2±0.2。42℃+1℃继续培养48h5.3分离
将24h增菌液、48h增菌液以及相应的1:50稀释液分别划线接种于Skirrow与mCCD琼胎平板上,微需氧条件下42℃士1℃培养24h~48h。另外,可同时选择使用CFA显色乎板。观察24h培养与48h培养的琼脂平板上的菌落形态。mCCD琼脂平板上的可疑菌落通常有光泽,潮湿、扇平,呈扩散生长的倾向,直径约为1tmm~-2mmSkirruw琼脂平板l的可疑菌落为灰色、巅平、润有光泽,呈沿接种线向外扩散的倾问;有些可疑菌落常皇分散凸起的单个菌落,直径约为1mm2mm,边缘整齐、发亮。CFA显色平板上的可疑菌落为红色、突起、湿润,菌落直径约为2mm~3mm,近缘有一圈红色的透明环,中间有:-个圆形的、不透明、颜色较深的红色小点的荫落。5.4鉴定
5.4.1鸾曲菌属的鉴定
挑取5个或更多的可凝菌落接种到哥伦比亚琼脂平板上,微需氧条件下42℃士1℃培养21h~48h,按照5.4.1.1~5.4.1.5进行鉴定,结果符合表1的可疑菌落确定为弯曲菌属。3
GB/T4789.9—2008
形态观察
动力观察
氧化醇实验
微需氧条件下25 ℃±1℃生长试验有氧条件下42℃±1℃生长实验
有些菌株的形态不典型。
b有些菌株的运动不明显。
5.4.1.1形态观察
表1弯曲菌属的监定
弯曲菌属性
莹兰氏阴性,菌体弯曲如小点状,两荫体的未端相接时呈S形、蝶旋状或海鸥展翅状”
圣现螺放状运动
不生长
不生长
挑可疑菌落进行革兰氏染色,镜检。5.4.1.2动力观察
挑取可疑菌落用1mI.布氏肉荡悬浮,用相养显微镜观察运动状态。5.4.1.3氧化酶试验
用铂/铱接种环或玻璃棒挑取可疑菌落至氧化悔试剂润湿的滤纸上,如果在10s内出现紫红色、紫罗兰或深蓝色为阳性。
5.4.1.4微需氧条件下25℃±1℃生长试验挑取可疑菌落,接种到哥伦比亚琼脂平板上,微需氧条件下25℃十1℃焙养44h土1h,观察细菌生长情况。
5.4. 1.5有氧条件下42℃±1℃生长试验挑取可疑菌落,接种到哥伦比亚琼脂平板上,有氧条件下42℃土1℃培养44h十4h,观察细菌生长情况。
5.4.2空肠弯曲菌的监定
5.4.2.1过化氢酶试验:挑取菌落,加到于净玻片上的3%过氧化氢溶液中,如果在30s内出现气泡则判定结果为阳性。
5.4.2.2马尿酸钠水解试验:挑取菌落,加到感有0.4mL1%马尿酸钠的试管中制成菌悬液。混合均匀后在36℃士1℃水浴放置2h或36℃士1℃培养箱中放置1h。沿着试管壁缓缓加入0.2mL节-酮溶液,不要振荡,在36℃±1℃的水浴或培养箱中放置10 min后判读结果。若出现深紫色则为阳性;若出现淡紫色或没有颜色变化则为阴性。5.4.2.3吲哚乙酸酯水解试验:挑取菌落至吲哚乙酸酯纸片上,再滴加一滴灭菌水。如果吲哚乙酸醋水解,则在5min~10min内出现深蓝色;若无颜色变化则没有发生水解。5.4.2.4药物敏感性试验(可选择):挑取菌落,在布氏肉汤中制备成浓度为0.5McFarlad的菌悬液,再用布氏肉汤制备1=10的稀释液,在5%MuellerHinton琼脂平板上进行涂布,静置5min后去除多余液体,将平板在36℃土1C培养箱中放置10rnin进行1燥。将头孢需素(30g)和萘啶酮(30μg)药敏纸片放在琼脂表面。将平板在微需氧条件下36℃土1℃培养22h土2h。如果细菌紧贴着纸片牛长则为有抗性;如果纸片周围山现不同程度的细菌抑制生长则为敏感。空肠弯曲菌的鉴定结果见表2。品成伴网ht
过氧化氢酶试验
马尿酸盐水解试验
吲哚乙酸酯水解试验
头孢菌素敏感试验
紫啶酮酸敏感试验
表 2 空肠弯曲菌的鉴定
空肠弯曲菌
(C. ieiu)
注+阴性;一阴性;S敏感;R抗性。结晰弯曲菌
(C. cpit)
空肠弯曲菌和结肠弯曲菌对禁啶酮酸的耐药性呈现出增长趋势。b 海鸥弯曲菌的不同菌株,分别表现为敏感或抗性。海鹏弯曲菊
tr. tari)
GB/T 4789.9—2008
乌·肾萨拉弯曲菌
(C. μpsatiensis)
-或微弱
5.4.2.5对于确定为弯帕属的菌落,可使用APICampy生化鉴定试剂盒或VITEK2NII牛化鉴定卡来替代5.4.2.1~5.4.2.4的鉴定,具体操作按照产品说明书进行。5. 5结果报告
综合以上试验结果,报告检样单位中检出空肠弯曲菌或未检出空肠弯曲菌。第二法全自动酶联荧光免疫分析仪筛选法6原理
弯曲菌的酶联荧光免疫筛选法是在全自动酶联荧光免疫分析仪1.进行的双抗体夹心酶联荧光免疫检验方法。固相容器(SPR)用抗弯曲菌抗体包被,各种试剂均封闭在试剂条内。煮沸过的增菌肉汤加人试条孔,在特定时间内样本在SPR内外反复循坏,使得弯曲菌抗原与包被在SPR内部的弯曲菌抗体结合,洗涤去除未结合的其他成分。接着标记有碱性磷酸酶的抗体与固定在SPR壁上的弯曲菌抗原相结合,洗去未结合的抗体标记物。结合在SPR壁上的碱性磷酸酶将催化底物磷酸4-甲基伞型物转变成具有荧光的4-甲基伞形酮,以450nm波长处检测荧光强度,出仪器分析后得出检验结果。7仪器
mini VIDAS或 VIDAS.
8试剂
8.1弯曲菌试剂条(VIDASCAM)。
8.2校正液:纯化灭活的弯曲菌抗原标准溶液。8.3阳性对照。
8.4阴性对照。
8.5 MLE卡.
操作步骤
9.1增菌液处理
取lmL24h培养的Bolton增菌液加人试替中,100℃水浴15min。剩余增菌液继续培养至48h,5
GB/T4789.9—2008
9.2仪器操作
9.2.1输入MLE卡信息
每个试剂盆在使用之前,首先要用试剂盒中的MLE卡向仪器输入试剂规格(或曲线数据)。每盒试剂只需输人次。
9. 2. 2 校正
在输入MI.-卡信息后,使用试剂盒内的校正液进行校正,校正应做双份测试。以后存14d进行次校正。
9.3检测
取出试剂条,待恢复至室温后进行样本编号。建立工作表格,输人样本编号,分别吸取500uL阴性、阳性对照和样本(冷却至室温)加人到试剂条样本孔中央。依照屏幕提示,将VIDAS CAM试剂条放入仪器的相应位置。所有分析过程由仪器自动完成。9.4结果报告
9.4.1检测值(X)是样品的相对荧光值(RFV.)与标准溶液的相对荧光值(RFV。)的比值,见式(1)X = RFV,
若检测值0.10,则检测结果为阴性;若检测值含0.10,则检测结果为阳性。(1)
9.4.2检测结果阴性,可直接报告检验单位中末检出空肠曲菌。检测结果阳性的样品,应按照5.3~5.4对剩余增菌液进行确认并报告。A,1Bolton肉汤(Bnltonhroth)
A. 1. 1 基础培养基
A.1.1.1成分
附录A
(规范性附录)
培养基与试剂
动物组织酶解物(enzymatic:digestalanimaltissues)乳白蛋白水解物(lauctalbuinhydrolysate酵母浸膏
氯化钠
丙酮酸钠
偏亚硫酸氢钠
碳酸钠
α-酮戊二酸
A,1,1.2 制法
1 000 mL
CB/T 4789.9—2008
用水溶解基础培养基成分,如需要可使用加热促其溶解。将基础培养基分装牟合适的锥形瓶内,121 ℃灭菌 15 min-
A.1.2无菌裂解脱纤维绵羊或马血对无菌脱纤维编羊或马血通过反复冻融进行裂解或使用皂角苷进行裂解,A.1.3抗生素溶液
A. 1.3. 1 成分
头孢哌酮(cefuperazae)
万古霉素(vuncomycin)
H甲氧芋胺嘧啶乳酸盐(trimethoprim lactate)两性莓蒸B(amphotercinB)
多粘菌素B(polymyxin B)
乙醇/灭菌水(50/50,体积比)A. 1. 3. 2 制法
将上述成分溶解于乙醇/菌水混合溶液中。A. 1. 4 完全培养基
A, 1. 4. 1 成分
基础培养基(A.1.1)
无菌裂解脱纤维绵羊或马血(A.1.2)抗牛素溶液(A,1.3)
1000 mL
A, 1.4. 2 制法
当基础培养基的温度约为45℃左右时,无菌加人绵羊或乃血和抗生素溶液,混勾,将完全培养基的pH值调至7.2士0.2(25℃),将培养基无菌分装至合适的试管或锥形瓶中备用。配制的增菌液在常温下放置不得超过4h,或在4左右避光保存不得超过7d。7
合品成伴网httn
GB/T4789.9—2008
A.2改良CCi)琼脂(modiriedcharcoalcefoperazonedeoxycholateagar,mCcDA)A.2.1基础培养基
A.2.1.1成分
肉浸液
动物组织酶解物
氯化钠
酪蛋白酶解物
去氧胆酸钠
硫酸业铁
丙酮酸钠
A. 2. 1.2制法
8, 0 g~18. 0 g
1000ml
用水溶解基础培养基成分,煮沸。分装至合适的三角瓶内,121℃高压灭菌15min。A,2.2抗生紊溶液
A.2.2.1成分
头孢葡(cefoperaznne)
两性霉素B(amphotericinB)
利福平(rilatmpicin)
乙醇/灭菌水(50/50,休积比)A. 2. 2. 2 制法
将述成分溶解于乙醇/灭菌水混合溶液中。A.2.3完全培养基
A, 2. 3. 1 成分
基础培养基(A.2.1)
抗生素溶液(A.2.2)
A,2.3.2制法
1000mL
当基础培养的温度约为15℃左右时,加人抗生素溶液,混匀。将完全培养基的pH值调至7.210.2(25℃)。倾注约15mL于无菌平血中,静置至培养基凝固。使用前需预先干燥平板。t将平皿盖打开,使培养基面朝下,置于于燥箱中约30min,直到琼脂表面于燥。预先制备的平板未十燥时在室温放置不得超过4l,或在4C左右冷藏不得超过7d.A.3哥伦比亚琼脂(Columbia bloodagar)A,3.1基础培养基
A.3.1.1成分
动物组织酶解物
氯化钠
合伙伴网
8. 0 g~18.0 g
1 000 mL
A.3. 1.2 制法
GB/T4789.9—2008
将基础培养基成分溶解于水中,加热促其溶解,分装至合适的三角瓶内,121℃高压灭菌151nit。A.3.2无菌脱纤维绵羊血
无菌操作条件下,将绵羊血加入到盛有灭菌玻璃珠的容器中,振摇约10min,静置后除去附有血纤维的玻璃珠即可。
A.3.3完全培养基
A.3.3. 1组分
基础培养基(A.3.1)
无菌脱纤维绵羊血(A.3.2)
A.3.3.2制法
1000tmL
当基础培养基的温度为45℃左右时,无菌加人缔羊血,混匀。将完金培养基的pFI值调至7.2士0.2(25℃)。倾注15mL十无菌平血中,静置至培养基凝固。使用前需预先干燥平板。可将平血盖打开,使培养基面朝下,置于干爆箱中约30rin,直到琼脂表面干燥。预先制备的平板末干燥时在窄温放置不得超过 4 h,或在 4 ℃左右冷藏不得超过 7 d。A.4布氏肉汤(Brucellabroth)A.4.1成分
酪蛋白酶解物
动物组织酶解物
葡萄糖
酵母浸音
氯化钠
亚硫酸氢钠
A, 4.2制法
1 000 mL
将基础培养基成分溶解丁水中,妇需要可加热促其溶解。将高压灭菌后培养基的pH值调至7.0十0.2(25℃))。将培养基分装至合适的试管中,每管10mL,121℃高压灭菌15min,A.5氧化酶试剂(reagentforthedetectionofoxidase)A.5.1成分
四甲基对苯一胺盐酸盐(N,N.N',N'-tetramcthyl-1,4-phenylenediaminedihydrochloride)蒸馏水
A.5.2制法
使用前迅速将上述成分溶于水中。1.0g
100 mL
A.6马尿酸钠水解试剂((reagents for the detection of hydrolysis of hippurate)A.6.1马尿酸钠溶液
A.6. 1. 1 成分
马尿酸钠
磷酸盐缓冲液(PBS)组分:
氯化钠(NaC1))
磷酸氢二钠(NaHPO,·2HzO)
小提示:此标准内容仅展示完整标准里的部分截取内容,若需要完整标准请到上方自行免费下载完整标准文档。